1. del: Potencialne koristi flavonoidov na napredovanje ateroskleroze z njihovim učinkom na razdražljivost žilnih gladkih mišic
Mar 22, 2022
Za več informacij kontaktirajtetina.xiang@wecistanche.com
Povzetek: Flavonoidi so skupina sekundarnih presnovkov, pridobljenih iz živil rastlinskega izvora, in nudijo številne koristi za zdravje v različnih fazah več bolezni. Ta pregled se bo osredotočil na njihove učinke na ionske kanale, izražene v gladkih mišicah žil med aterosklerozo. Ker je ionske kanale mogoče regulirati z redoks potencialom, je pričakovati, da med pojavom bolezni, povezanih z oksidativnim stresom, ionski kanali spremenijo svojo prevodno aktivnost, kar vpliva na napredovanje bolezni. Tipično stanje, povezano z oksidativnim stresom, je ateroskleroza, ki vključuje disfunkcijožilnigladka mišica. Naš cilj je predstaviti stanje tehnike o tem, kako redoks potencial vpliva na delovanje ionskih kanalčkov gladkih mišic žil in povzeti, ali koristi, opažene pri tej bolezni z uporabo flavonoidov, vključujejo obnovitev aktivnosti ionskih kanalčkov.
Ključne besede: flavonoidi; napredovanje; ateroskleroza; ionski kanali; žilni; gladka mišica; kalcijevi tokovi; oksidativni stres; membranski potencial; razdražljivost

1. Uvod
Ateroskleroza je glavni vzrokbolezni srca in ožilja[1,2]; te bolezni veljajo za prvi vzrok umrljivosti po vsem svetu, zlasti v razvitih državah in državah z visokim dohodkom, saj vsako leto vzamejo življenja skoraj 18 milijonov ljudi [3]. Ateroskleroza je bolezen, ki z leti napreduje in lahko prizadene kogar koli, brez rasnih ali spolnih omejitev; vendar genetski in okoljski dejavniki ogrožajo specifične populacije [4]. Zapleti te bolezni predstavljajo tudi visoke stroške za bolnike in zdravstvene sisteme. Zato je nujno, da si prizadevamo preprečiti napredovanje te bolezni [3,5,6]. Primarni preventivni ukrepi vključujejo izboljšanje prehranjevalnih navad. Diete, obogatene s polinenasičenimi maščobnimi kislinami in antioksidanti, z ustreznim vnosom vlaknin ter nizko vsebnostjo predelane hrane in nasičenih maščobnih kislin, so bile povezane z manjšo pojavnostjo srčno-žilnih bolezni. En primer je uživanje antioksidantov, kot so askorbinska kislina, karotenoidi, vitamin E in polifenoli. Številne študije kažejo na koristi uživanja sadja in zelenjave, ki vsebujeta antioksidante, znane kot flavonoidi [7,8].
Flavonoidiso sekundarni metaboliti iz rastlin in največja skupina polifenolnih spojin. Obstaja več kot 5000 različnih flavonoidov z različnimi aktivnostmi. Polifenole so veliko preučevali, vse odkar jih je leta 1930 odkril Albert Szent-Gyorgyi, ko je izoliral citrin iz limone in ga poimenoval vitamin P. To ime je bilo izbrano, ker je molekula uravnavala prepustnost kapilar [9]. Flavonoide zaužijemo v redni prehrani, ko vsak dan uživamo sadje in zelenjavo |10]. Razdeljeni so v podskupine: halkoni, avroni, flavoni, flavanoli, antocianidini, flavonoli, flavanoni in izoflavoni [11]. Imajo skupne značilnosti, ki jim dajejo visoko hranilno vrednost, čeprav predstavljajo razlike v absorpciji, metabolizmu in biološki uporabnosti [12]; vsi imajo znatne koristi za zdravje ljudi, če jih redno uživamo. Pomoč pri zdravju ožilja je posledica njihove biološke aktivnosti kot antioksidantov od nasprotovanjaoksidativni streszmanjša tveganje za razvoj ateroskleroze [13]. Nekatera od teh dejanj izhajajo iz njihove interakcije z reaktivnimi kisikovimi vrstami (ROS) in reaktivnimi dušikovimi vrstami (RNS); vendar pa so poročali tudi o učinkih na ionske kanale v plazemski membrani endotelijskih in vaskularnih gladkih mišičnih celic [13,14].
Ionski kanalčki so sestavni proteini v plazemskih in notranjih membranah. Odgovorni so za gibanje ionov skozi membrane, imenovane ionski tokovi. Ti tokovi povzročajo spremembe v električnih lastnostih celic, kot so endotelijske in vaskularne gladke mišične celice (VSMC) v žilah. Mnoga od teh neravnovesij vplivajo na znotrajcelične koncentracije kalcija, kar moti regulacijo krčenja in sproščanja žil [14]. VSMC sestavljajo stenske žile in nadzorujejo premer srednjih in velikih krvnih arterij. Ta skupina celic se skrči ali sprosti, da ohrani krvni tlak in oksigenacijo tkiv. Ko se v žilah začne kopičiti oksidirani holesterol, se razvije ateroskleroza, ki povzroča srčne zaplete in različne periferne žilne bolezni z visoko stopnjo obolevnosti in umrljivosti [11,15].
Ta članek obravnava vpliv ionskih tokov vaskularnih gladkih mišic na napredovanje ateroskleroze in kako je mogoče to spremenjeno stanje obrniti z uporabo flavonoidov.

2. Ateroskleroza
Ateroskleroza je imunsko-presnovna bolezen, ker prizadene celice imunskega sistema in organske molekule presnove. Aterosklerotične lezije kažejo velike količine monocitov, makrofagov, lipoproteinov in holesterola nizke gostote. Napredovanje bolezni se šteje za kronično. Gre za degenerativni proces, ki poteka v več fazah. V stenah krvnih žil nastanejo poškodbe zaradi kopičenja lipidov, kalcija, trombocitov in drugih krvnih spojin [16]. Proces razvoja plakov poteka v koronarnih, aortni, karotidnih, iliakalnih in femoralnih arterijah več let[17]. Proces se začne z zgodnjim razvojem maščobnih prog v otroštvu; potem se zgodnji fibroaterom oblikuje v adolescenci in dvajsetih letih. Napredovali aterom ali tanka kapica fibroateroma se pojavi pri starejših nad 55 let [18].
2.1. Splošni koncepti
Patogenezo ateroskleroze lahko povzamemo v štirih hipotezah: (a) oksidativna modifikacija lipoproteinov nizke gostote (LDL) [19, 20], (b) odziv na poškodbo [21], (c) odziv na zadrževanje LDL [22, in (d) avtoimunska narava bolezni [23, 24] (slika 1). Dva poskusa podpirata hipotezo o oksidativni modifikaciji LDL: najprej je bilo dokazano, da oksidirani LDL (ox-LDL) povzroča poškodbe gojenih endotelijskih celic [25, 26; drugič, ox-LDL so prepoznali različni čistilni receptorji (lektinu podoben oksidirani LDL receptor-1(LOX-1), vključno z čistilnimi receptorji, ki vežejo LDL(CD36), čistilnimi receptorji za fosfatidilserin in oksidirani LDL pri ljudeh aterosklerotičnih lezij (SR-PSOX) in multifunkcionalnega receptorja pri aterosklerozi (makrofagni receptorji SR-A), ki posreduje vtok lipidov v makrofage.Aktivacija vseh teh receptorjev je spodbudila nastanek penastih celic v gojenih endotelijskih celicah [27].
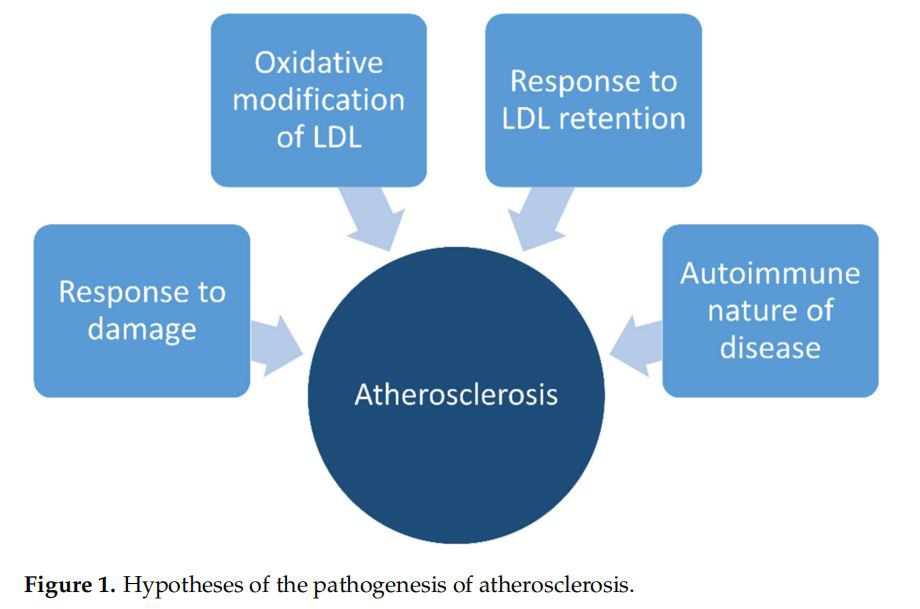
Druga hipoteza meni, da je škoda, povzročena nažilniendotel je odgovoren za aktivacijo endotelija in začetek aterosklerotičnega procesa. Proces je vključeval povečano prepustnost lipoproteinov in izražanje adhezijskih molekul, kot so E-selektin, P-selektin, adhezijska molekula vaskularnih endotelijskih celic-1(VCAM-1) in medcelična adhezijska molekula{{ 4}} (ICAM-1). Te molekule se vežejo na svoje ustrezne receptorje na krožečih monocitih in limfocitih T ter inducirajo novačenje teh celic na mesto poškodbe, kjer vrste ROS iz fibroblastov in drugih celic povzročijo aterogenezo [28].
Tretja hipoteza najprej obravnava zadrževanje LDL. Kopičenje lipoproteinov znotraj arterijske stene in arterijskih proteoglikanov lahko sproži pro-vnetno kaskado in spodbuja aterosklerozo [29, 30]. Četrta hipoteza je povezana z avtoimunsko naravo bolezni; to vključuje imunski odziv pred razvojem plakov. Med zagonom bolezni sodelujejo antigeni, protitelesni kompleksi, limfociti T, limfociti B in proteini sistema komplementa ter infiltracija mononuklearnih celic v lezijo, kot so CD8 plus limfociti, CD4*(Th1) pomožni limfociti T, mastocitov, monocitov in makrofagov. Pojavijo se DAMP (molekulski vzorci, povezani s poškodbami), kot so proteini toplotnega stresa (HSP) in ox-LDL; pravzaprav se lahko protitelesa proti HSP60 uporabijo kot marker bolezni za napredovanje. Prirojene imunske celice prepoznajo ox-LDL in HSP in se aktivirajovnetje; vsi ti dogodki podpirajo pomen imunosti med razvojem bolezni [31-33].
Vsak od teh štirih procesov povzroča aterosklerozo, vendar jo je mogoče preprečiti z zmanjšanjem dejavnikov tveganja. Glavni aterogeni dejavniki tveganja so centralna debelost, oksidativni stres, dislipidemija, hiperglikemija in provnetna stanja 34,35]. Študije so poročale, da so visoke serumske koncentracije LDL-holesterola, glukoze in C-reaktivnega proteina (CRP) neposredno povezane s tveganjem za razvoj srčno-žilnih bolezni [35,36].
Treba je razumeti podrobnosti patofiziologije bolezni, da razvijemo ustrezne preventivne in/ali terapevtske strategije, s katerimi se lahko izognemo vaskularni kalcifikaciji [37J. Med tem procesom so prevladujoča vrsta celic v arterijski steni celice gladkih mišic; odgovorni so za strukturo in celovitost delovanja žil [21]. Kalcifikacija nastane v intimi krvnih žil na določenih točkah, ki tvorijo kristalne zaplate z nekrotičnimi prostori jedra [37,38]. Med začetnim stadijem ateroskleroze gladke mišične celice predstavljajo 90 odstotkov celične vsebine na območju lezije. Vendar se to spremeni pri napredovalih lezijah; v teh primerih zunajcelični matriks prevladuje nad gladkimi mišičnimi celicami, ki tvorijo vlaknasto oblogo plakov. Celice gladkih mišic z neproliferativnim kontraktilnim fenotipom se spremenijo v celice, ki aktivno proliferirajo, migrirajo, ki jih pritegnejo kemotaktična sredstva, in proizvajajo proteine zunajceličnega matriksa (kolagen, elastin in proteoglikane). Ta transformacija aktivira izražanje genov, ki kodirajo membranske receptorje za rastne faktorje [22]. Migracija gladkih mišičnih celic spodbuja kalcifikacijo na poškodovanem območju, kar je povezano z višjo stopnjo umrljivosti in obolevnosti [39].
Spontana ruptura aterosklerotičnega plaka povzroči aktivacijo protrombotičnih elementov endotelija. Ko se trombociti agregirajo, sprostijo zrnca, bogata z mitogeni, in inducirajo migracijo in proliferacijo gladkih mišičnih celic, vključno z vnetjem in oksidativnim stresom, ki sta prisotna v vseh fazah bolezni [40,41].
2.2. Stopnje ateroskleroze
Obstaja način za razvrstitev napredovanja ateroskleroze na podlagi histoloških študij obdukcij ljudi in živali v naslednje faze: predateroskleroza, zgodnja ateroskleroza, pozna ateroskleroza in klinične posledice [42,43]. V vseh fazah so celice gladkih mišic žil ključnega pomena za razvoj plakov. Predateroskleroza se začne ob rojstvu, ker se difuzne zadebelitve intime in ksantomi intime uporabljajo kot prilagoditev na pretok krvi[44-46]; to velja za predplak [42]. Med zgodnjo aterosklerozo nastane patološka zadebelitev intime. Ta zgodnji plak vsebuje zunajcelične lipidne bazene globoko v intimi z veliko količino VSMC in zunajceličnega matriksa (ECM)[42,43]. Napredovanje vključuje zadrževanje in oksidacijo LDL, indukcijo vnetja in proliferacijo VSMC s fenotipskimi spremembami in smrtjo [22, 47]. VSMC proizvajajo ECM v intimi, kjer igra bistveno vlogo pri začetku ateroskleroze. Med tem procesom je bilo dokazano, da negativno nabite stranske verige proteoglikanov interagirajo s pozitivno nabito stranjo apolipoproteinov [48], da zadržijo lipoproteine iz plazme [30]. Ujeti lipoproteini trpijo zaradi oksidacije, rekrutirajo se makrofagi in začne se vnetje [22]. Včasih pride do mikrokalcifikacije v bližini medijskega tkiva, ki je povezana z apoptozo VSMC [49]. Patološka zadebelitev intime v poznih fazah je vedno prisotna z obilnimi makrofagi, kar predstavlja ključni korak za napredovanje v fibroaterom [50-54] in proliferacijo, migracijo in spremembo fenotipa VSMC [55]. V poznih fazah je potrebno kopičenje makrofagov v luminalnem prostoru. Za lezijo je značilna fibrozna kapica in nekrotično jedro, ki ga tvorijo mrtvi VSMC in makrofagi, ki fagocitirajo lipide in postanejo penaste celice [56,57]; nato se razvije fibroaterom in kalcifikacijo lahko opazimo najprej v nekrotičnem jedru in nato v okoliškem ECM [58-60]. Ta zreli plak tvori liste, katerih delci lahko štrlijo v lumen in povzročijo trombozo [42, 60]. Končno so klinične posledice odvisne od tega, katera arterija je bila prizadeta [6].
2.3. Vloga oksidacije
ROS in RNS vrste se proizvajajo v nizkih koncentracijah v VSMC, adventitiji in endotelijskih celicah v normalnih pogojih. Delujejo kot posredniki pri celičnem signaliziranju za uravnavanje vaskularne aktivnosti [13,62-64], sodelujejo pri rasti gladkih mišic žil ter uravnavajo krčenje in sprostitev [65,66]. Vendar pa med patološkimi stanji obstaja neravnovesje med antioksidanti in oksidanti, in ko so oksidanti naklonjeni, nastane oksidativni stres. Viri ROS vključujejo lipooksigenaze, citokrom P450, ciklooksigenazo, ksantin oksidazo, mitohondrijsko dihanje, NADPH oksidazo in nevezane sintaze dušikovega oksida [13]. Poleg tega lahko znotrajcelična proizvodnja ROS izhaja iz verige prenosa elektronov [67]. Eno prvih tkiv, prizadetih pri aterosklerozi, je endotelij, kjer nastajajo dušikov oksid (NO), endotelin I, angiotenzin II, adhezijske molekule in citokini [13,68]. Oksidativni stres vpliva na celične funkcije, povzroča endotelijsko disfunkcijo in zmanjša sintezo NO; zmanjšana biološka uporabnost NO ima aterogene učinke [69]. Pomemben dejavnik, ki ni bil globoko raziskan, je, kako oksidativni stres modulira oksidacijo ionskih kanalov v VSMC med razvojem ateroskleroze. Ionski kanali predstavljajo transcendentalne elemente za pravilno delovanje VSMC; če je njihova funkcija ogrožena, je pomembno razjasniti, kako to vpliva na razvoj bolezni [70].
ROS in RNS lahko neposredno ali posredno vplivata na ionske kanale: neposredno s proizvodnjo posttranslacijskih modifikacij na proteinih, kot je nitrozilacija, sulfhidracija ali nitracija specifičnih aminokislinskih ostankov; ali posredno s spreminjanjem različnih signalnih poti. Atomi žvepla v cisteinu in metioninu dajejo občutljivost na redoks potenciale kot tudi na aromatske obroče iz histidinskih, fenilalaninskih, triptofanskih in hidroksilnih skupin v ostankih tirozina [14]. Visoka reaktivnost tiolnih skupin cisteina prispeva k tvorbi sulfenske kisline, sulfinske kisline ali sulfonske kisline, odvisno od koncentracije oksidanta in reakcijskih pogojev; metionin tvori metionin sulfoksid in metionin sulfon; histidin oksidira v 2-heksahistidin, triptofan pa oksidira v 5-hidroksitriptofan in oksindolealanin [71]. Cistein lahko utrpi druge modifikacije, kot sta nitrozilacija in glutationilacija [70]. Na primer, v vaskularnih gladkih mišičnih celicah lahko ROS in NO oksidirata napetostno odvisne kalcijeve kanale Cav1.2b cisteinske ostanke znotraj podenote alfa in povzročita konformacijske spremembe [14].

2.4. Poškodbe gladkih mišičnih celic žil
Gladke mišične celice žil imajo razlike v izražanju signalnih proteinov, receptorjev in ionskih kanalov v primerjavi s srčno in skeletno mišico. Njegova kontraktilnost je bistveno drugačna, ker VSMC ne izvajajo akcijskega potenciala. V mirovanju so delno skrčene, kar poveča njihovo kontraktilnost kot odgovor na nevronske, humoralne ali endotelne dražljaje, ki delujejo na membranske receptorje. Ta kontraktilnost je razmeroma počasna in je včasih lahko vzdržljiva in tonična [72]. Vzdrževanje žilnega tonusa je pod nadzorom membranskega potenciala VSMC. Depolarizacija aktivira visokonapetostno odvisne kalcijeve kanale tipa L (Cav1.2) na plazemski membrani, kar sproži povečanje vstopa Ca2 plus [73]
Povečanje intracelularnega Ca2 spodbuja kontraktilni odziv z aktiviranjem od kalcijevega kalmodulina odvisne miozinske lahke verige kinaze (MLCK) in sproščanjem več Ca2 plus iz znotrajceličnih zalog kalcija [74]. Po drugi strani iztok K plus skozi Ca2 plus -aktivirane K kanale (KCa) posredno modulira membranski potencial, ker omejujejo pretok Ca2 plus ionov v celice, kar povzroča inhibicijo Cav1.2 [75]. Celična membrana gladkih mišic žil vsebuje številne vrste kanalov. Med kalcijevimi kanali imamo kot glavne regulatorje kanale tipa L, kot je Cav1.2b, ki je drugačna izoforma od Cav1.2a v srčni mišici [14]. So glavni regulatorji gladkih mišic žil [Ca2] I in kontraktilnosti. Ti kanali delujejo na dveh različnih ravneh: depolarizacija in hiperpolarizacija. Skupina, zadolžena za depolarizacijo, vključuje družino prehodnega receptorskega potenciala (TRP), kanale TRPC3, TRPC6 in TRPM4, skupina, ki spodbuja hiperpolarizacijo, pa vključuje kalcijeve kanale, aktivirane s pomembno prevodnostjo, kanale TRPV4 in Cav3.2. Vstop kalcija v celico pretežno posredujejo kanali tipa L (Cav1.2b) in do neke mere kanali tipa T Cav3.1/3.3; nadzorujejo kontrakcijo, njihovo aktivnost pa uravnavajo spremembe v membranskem potencialu [76].
Drugi kanali v plazemski membrani vključujejo kloridne kanale. Imajo več funkcij, vključno z regulacijo celičnega volumna, transepitelnim transportom, ionsko homeostazo in regulacijo električne vzdražnosti [77]. V gladkih mišičnih celicah je elektrokemijski potencial za klorid višji od potenciala mirovanja. Nato lahko odpiranje kloridnih kanalov povzroči dovolj depolarizacije, da povzroči aktivacijo Cav kanalov in Ca2 plus dotok, kar je pomembno za vaskularni odziv na mehanski stres [78].
Membranski ionski kanali VSM so razvrščeni na naslednji način:
(a) Napetostno odvisni Ca kanali (VGCC).Ti kanali uravnavajo kontrakcijo in izražanje genov v VSCM. Ca kanali L-tipa in T-tipa so reprezentativni člani te družine. Ko se aktivirajo kanali tipa L, se membrana depolarizira in kalcijevi ioni vstopijo v citoplazmo; nato se aktivirajo kalijevi kanalčki in pride do hiperpolarizacije membrane s kasnejšo deaktivacijo VGCC [79]. Aktivacija PKG prispeva k vazodilataciji, ki jo posreduje NO, in zavira tokove Cav1.2 [80].
Kanali tipa T lahko prispevajo k miogenemu tonusu pri nizkem intravaskularnem tlaku, ko so gladke mišične celice relativno hiperpolarizirane; vendar pa je treba njihovo posebno vlogo dodatno pojasniti [81].
(b)Ca2-aktivirani K-kanali (KCa).Ti kanali se aktivirajo s povečano Ca2 in znotrajcelično koncentracijo; BKC je največ v VSMC. Do zdaj sta samo dve študiji identificirali kalijeve kanale, aktivirane s kalcijem (SK Ca) z majhno prevodnostjo v VSMC iz sistemskih krvnih žil [82], kalijeve kanale, aktivirane s kalcijem (IKCa) z vmesno prevodnostjo, pa se izražajo samo v proliferirajočih VSMC [83]. .
(c) Napetostno odvisni kanali K plus (Kv).Prispevajo k mirujočemu tonusu malih koronarnih arterij in imajo dilatacijski učinek v koronarnem obtoku. Kv1.X je glavna skupina napetostno odvisnih kalijevih kanalčkov v VSMC koronarnih mikrožil. Identificirani družinski člani v žilnem sistemu vključujejo Kv1.2 in Kv1.5. Visoka proizvodnja peroksinitrita pri hiperglikemiji vpliva na te Kv kanale in poslabša vaskularno dilatacijo gladkih mišic [84]. Uravnavajo pljučno cirkulacijo in uravnavajo preoblikovanje žil v gladkih mišičnih celicah pljučne arterije [71].
(d) prehodni receptorski potencialni kanal (TRP).Na podlagi homoloških zaporedij je ta vrsta kanala razdeljena na šest členov: kanonični (TRPC1-7), melanostatin (TRPM1-8), vaniloid (TRPV1-6), ankirin (TRPA1), policistin (TRPP1-3) in mukolipin (TRPML1-3). Vsaka družina ima razlike v lastnostih in strukturi [85].
Tabela 1 prikazuje najbolj reprezentativne kanale, prisotne v VSMC, kako nanje vpliva oksidativni stres, posledice v membranskem potencialu in kako sodelujejo pri aterosklerozi.

Poleg tega je razdražljivost gladkih mišic posredno modulirana s citoplazmatsko koncentracijo kalcija, ki se sprošča iz mitohondrijev in sarkoplazmatskega retikuluma [86].
2.5. Naravne spojine za zdravljenje ateroskleroze
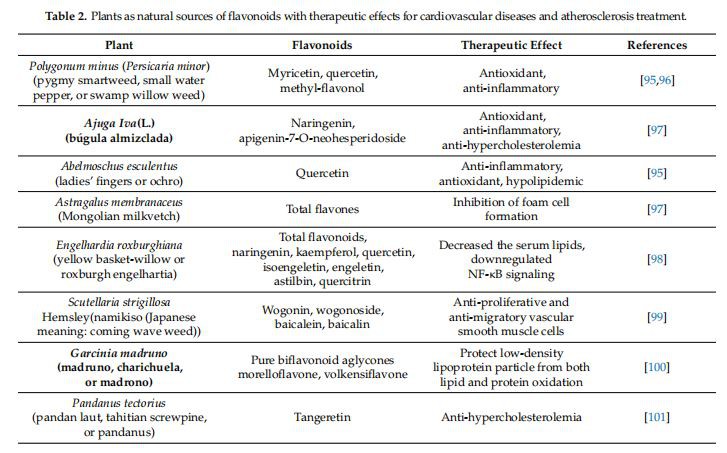
Številni rastlinski derivati se uporabljajo kot zdravila; njihove prednosti vključujejo manj sekundarnih učinkov in zmanjšanje oksidativnega stresa, ravni holesterola LDL in vnetja [87]. Uporaba naravnih spojin pri aterosklerozi je osredotočena na preprečevanje ali zdravljenje za zmanjšanje ravni lipidov v krvi. Med različnimi testiranimi snovmi je bilo ugotovljeno, da uživanje polifenolnih spojin, kot so flavonoidi, pomaga zmanjšati razvoj ateroskleroze zaradi močnega antioksidativnega delovanja [88], Sredozemska prehrana, ki vključuje uživanje oljčnega olja in oreščkov, zmanjšuje srčno-žilne incidenco bolezni za 30 odstotkov v primerjavi z dietami z nizko vsebnostjo maščob, ki so povezane z visoko vsebnostjo fenolov [89]. Zmanjšanje območja aterosklerotične lezije so opazili pri zdravljenju s flavonoidi v različnih študijah ex yivyo na aortah modificiranih Apo E miši [o0-o4] Povzetek različnih koristnih učinkov flavonoidov pri boleznih srca in ožilja je prikazan v tabeli 2.

Za dodatne informacije kliknite povezavo
https://www.xjcistanche.com/news/part2-potential-benefits-of-flavonoids-on-the-55147397.html
