Žilna prepustnost: regulacijske poti in vloga pri boleznih ledvic
Jul 26, 2022
Za več informacij. stiktina.xiang@wecistanche.com
Povzetek
Ozadje: Vaskularna prepustnost(VP) je temeljni vidik vaskularne biologije. Vse več študij je razkrilo, da številne signalne poti urejajo VP v fizioloških in patofizioloških pogojih. Poleg tega nastajajoči dokazi opredeljujejo spremembo VP kot ključni patogeni dejavnik priakutna poškodba ledvic, kronična ledvična bolezen, diabetična bolezen ledvicin druge proteinurične bolezni. Zato je zaznavanje povezav med temi potmi in etiologijo bolezni ledvic pomembna naloga, saj lahko takšno znanje sproži razvoj novih terapevtskih ali preventivnih medicinskih pristopov. V zvezi s tem je razprava, ki povzema poti, ki urejajo VP, in jih povezuje z boleznimi ledvic, zelo upravičena.
Povzetek: Glavne poti regulacije VP obsegajo angiogene dejavnike, vključno z vaskularnim endotelijskim rastnim faktorjem/VEGFR, angiopoetinom/Tie in semaforinom/nevropilinom razreda 3 ter vnetne dejavnike, vključno s histaminom, faktorjem aktivacije trombocitov in ekstravazacijo levkocitov. Te poti delujejo predvsem na vaskularni endotelijski kadherin, da modulirajo adherenske spoje endotelijskih celic (EC), s čimer povečajo VP preko paracelularne poti. Povišan VP pri različnih boleznih ledvic vključuje apoptozo EC, neuravnotežene regulacijske dejavnike in številne druge patofiziološke dogodke, kar posledično poslabša strukturne in funkcionalne motnje ledvic. Ukrepi za izboljšanje VP učinkovito izboljšajo obolelo ledvico v smislu poškodbe tkiva, endotelijske disfunkcije, delovanja ledvic in dolgoročne prognoze.
Ključna sporočila: (1) Angiogenski dejavniki, vnetni dejavniki in adhezijske molekule predstavljajo glavne poti, ki uravnavajo VP. (2) Vaskularna hiperprepustnost povezuje različne patofiziološke procese in ima škodljivo vlogo pri številnih boleznih ledvic. 2021 S. Karger AG, Basel
Ključne besede: Vaskularna prepustnost·Vaskularni endotelijski kadherin·Akutna ledvična poškodba·Kronična ledvična bolezen·Diabetična ledvična bolezen

Kliknite tukaj, če želite izvedeti, za kaj se uporablja cistanche
Uvod
Pri vretenčarjih ima žilni sistem nepogrešljivo vlogo pri shranjevanju krvi, hranjenju tkiv s kisikom in hranili, transportu presnovkov in ponujanju prehodov v imunski sistem. Za izpolnitev teh nalog zagotavlja ustrezne vmesnike in zadostno prepustnost za izmenjavo materiala med krvnim obtokom in različnimi tkivi [1].
Vaskularna prepustnost (VP) je na splošno opredeljena kot sposobnost krvnih žil, da nadzorujejo dvosmerni prehod molekul in imunskih celic z določenim razponom velikosti ter omejijo ekstravazacijo večjih molekul. V fizioloških pogojih molekule<40 kda="" can="" pass="" through="" mature="" vessels,="" whereas="" larger="" proteins,="" such="" as="" albumin="" (66="" kda)="" and="" transferrin(80="" kda),="" are="" retained.="" however,="" under="" pathophysiological="" conditions,="" for="" instance,="" inflammation,="" and="" allergy,="" even="" molecules="" of2,000="" kda="" may="" extravasate.="" in="" addition="" to="" size="" and="" physiological="" status,="" vp="" is="" also="" affected="" by="" the="" type="" of="" microvessels="" involved="" (venules="" or="" capillaries),="" other="" characteristics="" of="" the="" molecule(shape,="" charge,="" and="" hydrophilicity),="" and="" the="" histological="" pathway(transcellular,="" paracellular,="" or="" via="">
Vaskulatura ledvic je edinstvena in zapletena: ledvična arterija vstopi v ledvico pri ledvičnem hilumu in se naprej razveja v interlobularne in arkuatne arterije, ki sčasoma tvorijo glomerularne kapilare in postglomerularne kapilare. Ta specifična vaskulatura zagotavlja ultrafiltracijo krvi, proizvodnjo urina in vzdrževanje tekočinskega, elektrolitskega in kislinsko-bazičnega ravnovesja v ledvicah [3]. Kot vitalna lastnost vaskulature ledvic ima VP tako glomerulnih kot postglomerularnih kapilar ključno vlogo pri homeostazi ledvic. Glomerularna prepustnost filtracijske pregrade določa vrste molekul, ki jih je treba filtrirati iz seruma v Bowmanovo kapsulo. Poleg tega je VP postglomerularnih kapilar, vključno s peritubularno kapilarno mrežo in vasa recta, bistvenega pomena za reabsorpcijo ultrafiltrata in vzdrževanje medularnega osmotskega gradienta [4].
Sprememba VP je tesno povezana z različnimi boleznimi ledvic. Pri akutni ledvični poškodbi (AKI) kapilarna hiperpermeabilnost prispeva k mikrovaskularni hipoperfuziji, edemu, hipoksiji in vnetju, kar dodatno poslabša poškodbo tkiva in disfunkcijo [5]. Spremembe sistemske in glomerulne permeabilnosti so povezane z albuminurijo in edemom pri številnih proteinuričnih boleznih, kot so diabetične bolezni ledvic (DKD), idiopatski nefrotski sindrom (INS) in hipertenzija [6-8]. Za kronično ledvično bolezen (CKD), zlasti končno ledvično odpoved (ESRD), so poročali o mikrovaskularnem uhajanju, ki ga spremlja redčenje kapilar in tubulointersticijska fibroza, pri živalih in bolnikih, kar je povezano s slabo prognozo [9, 10].
Glede na ključno vlogo VP v homeostazi ledvic v fizioloških in patoloških pogojih je nadaljnja raziskava njegovega regulacijskega mehanizma in njegove povezave z boleznimi ledvic zelo upravičena. Ta pregled bo razpravljal o trenutnem napredku raziskav regulacije VP po glavnih signalnih poteh, spremembi VP pri različnih boleznih ledvic, njihovi korelaciji in prenosu takih molekularnih mehanizmov v predklinično in klinično prakso. Elementi in poti VP v ledvičnih kapilarah so povzeti na sliki 1.
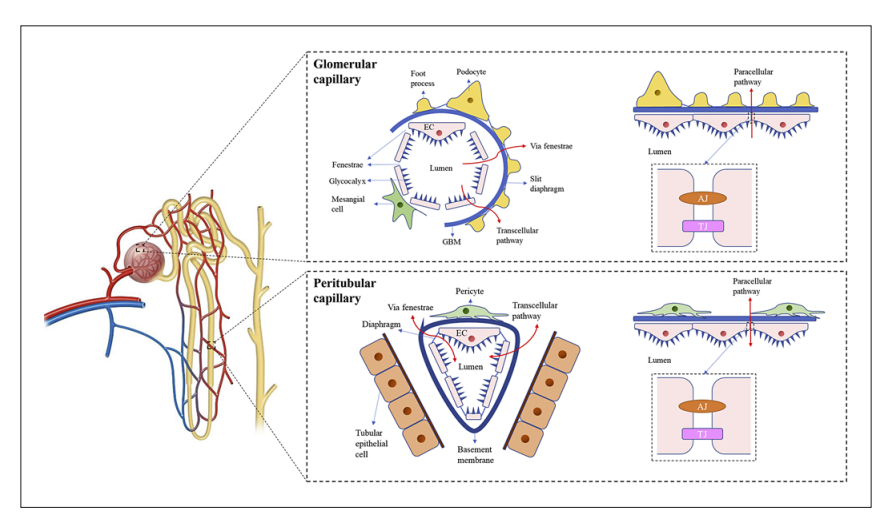
Slika 1. Ledvične kapilarne postelje in prepustne poti. Shematski povzetek elementov in poti VP v ledvičnih kapilarah. Ledvica ima dve vrsti kapilar, glomerularno kapilaro in postglomerularno kapilaro (peritubularna kapilara), ki imata različne elemente, ki vplivajo na njihovo prepustnost. Oba vključujeta endotelijski površinski glikokaliks in EC monosloj za transcelično pot, EC stičišča (TJ in AJ) za paracelularno pot, EC fenestre (peritubularne kapilarne fenestre imajo tanko diafragmo), pericite (mezangialne celice kot glomerularni periciti), in bazalno membrano (GBM). Poleg tega glomerularna prepustna pregrada vključuje podocite z razrezano diafragmo med njihovimi nožnimi procesi. VP, žilna prepustnost; EC, endotelne celice; TJ, tesni stiki; AJ, adherens spoji; GBM, glomerularna bazalna membrana.
Ureditev VP
Signalna pot VEGF/VEGFR
Vaskularni endotelijski rastni faktor (VEGF) je bil sprva imenovan faktor vaskularne prepustnosti, kar kaže na njegovo ključno vlogo pri regulaciji prepustnosti. Člani družine VEGF obsegajo VEGF-A do VEGF-E in placentne rastne faktorje, ki delujejo prek svojih receptorjev VEGFR1, VEGFR2 in VEGFR3 ter koreceptorjev nevropilina-1 (NRP1) in nevropilina-2(NRP2) [11].
VEGF-A/VEGFR2 s koreceptorjem NRP1 je glavna pot za modulacijo angiogeneze in VP [11]. V ledvicah VEGF proizvajajo predvsem podociti in tubularne epitelne celice, VEGFR2 pa se izraža na endotelijskih celicah (EC), kjer tvori mehanosenzorični kompleks z vaskularnim endotelijskim kadherinom (VE-kadherin), glavnim adhezivnim proteinom na stičiščih adherenov (AJ). Stimulacija VEGF sproži fosforilacijo VEGFR2 na tirozinu Y949, ki veže adapter, specifičen za T-celice, in nadalje sproži Src/ Signal Vav2/Race/PAK1, ki vodi do fosforilacije VE-kadherina pri Y658 in Y685 in nato do endocitoze, ki ji sledi razgradnja ali recikliranje, s čimer se poveča VP [12, 13]. Drugo fosforilacijsko mesto VEGFR2, odgovorno za VP, je Y1173, ki lahko prek PLC-odvisnega vtoka kalcija s fosforilacijo endotelne sintaze dušikovega oksida (eNOS), inducirane s potjo PI3K/Akt, pri serinu S1177, ac zasebni eNOS za proizvodnjo NO [12]. NO inducira vazodilatacijo in lokalno povečanje pretoka krvi, kar povzroči spremenjen strižni stres za modulacijo fosforilacije VE-kadherina in spremembo hidrostatičnega tlaka za spodbujanje intravaskularne ekstravazacije komponent [14,15]. Poleg tega NO posreduje S-nitrozilacijo -katenina pri Cys619, spodbuja njegovo disociacijo od VE-kadherina in razgradnjo AJ [16]. Tudi pot VEGF/VEGFR2 lahko posreduje VP prek motenj tesnih stikov (TJs) [17].
Zanimivo je, da je prej veljalo, da VEGFR3 s koreceptorjem NRP2 nadzoruje limfangiogenezo, vendar lahko VEGFR3 modulira tudi VP z zaviranjem ekspresije VEGFR2 in aktivnosti poti VEGF/VEGFR2 v mirujočih, angiogenih EC [18]. Tak pojav implicira interakcijo med VEGFR in poudarja njihov sintetični učinek pri osredotočanju na katero koli od teh poti, čeprav VEGFR predstavljajo neskladno afiniteto za različne ligande. Omeniti velja, da so zgoraj obravnavani podatki ustvarjeni z uporabo mišjih modelov [12-18] in EC, gojenih in vitro, vključno s človeškimi [14,15,17] in mišjimi [14-16,18]EC linijami, ki lahko ne odraža popolnoma procesa prenosa signalov v človeškem telesu. Poleg tega je treba poudariti, da internalizacija VE-kadherina kot skupne poti VP, ki jo povzroča VEGF, vodi do motenj AJ in končno posreduje VP prek paracelularne poti.

Angst/Neodločeno in VE-PTP
Angiopoetini (Angpts) so izločeni rastni faktorji, ki uravnavajo angiogenezo in vnetje preko endotelne receptorske tirozin kinaze Tie. Angel in Angpt2 delujeta antagonistično pri modulaciji VP: Angptl se konstitutivno izraža v ne-EC, fosforilira Tie2 na EC, spodbuja njegovo prerazporeditev in nadalje izzove pot Rapl/Race, da deaktivira fosforilacijo lahke verige miozina, posredovano s potjo RhoA/ROCK, preureditev VE-kadherina in vaskularno uhajanje [19,20]. Nasprotno pa je izražanje Angpt2 z EC običajno nadzorovano na nizkih ravneh, vendar je v patoloških pogojih regulirano navzgor in se konkurenčno veže na Tie2, da ga inaktivira [20]. Prav tako Angpt2 zmanjša izražanje claudina-5 v TJ, poveča izražanje caveolina-1 za podporo transcelularni poti in spodbuja odvajanje pericita in migracijo za posredovanje VP [21]. Drug možen mehanizem VP, ki ga povzroča Angpt2-, lahko vključuje poškodbo endotelnega površinskega glikokaliksa, ki je pomemben za endotelijsko disfunkcijo, saj klinično preskušanje kaže, da lahko povečan Angpt2 posreduje povezavo med lipoproteinom nizke gostote in holesterolom ter poškodbo glikokaliksa označen z biomarkerjem sindekan-l pri bolnikih z nefrotskim sindromom [22]. Tiel je manj značilen kot Tie2, ki bi lahko neposredno vplival na Tie2 za uravnavanje poti Angpt/Tie2, njegova delecija pa zaostri AJ s povečano ekspresijo VE-kadherina [23].
Vaskularna endotelna proteinska tirozin fosfataza (VE-PTP) je endotelijska specifična fosfataza, povezana z VE-kadherinom in Tie2, in stabilizira VE-kadherin v mirujočem endoteliju z zaviranjem GEF-H1-posredovane aktivacije RhoA in v aktiviran endotelij z defosforilacijo VE-kadherina pri Y658/Y685 [24]. Kontroverzno je, da lahko igra dvojno vlogo v izzvanem endoteliju, kjer njegova inhibicija aktivira Tie2 za stabilizacijo AJ. Vendar pa v odsotnosti Tie2 inhibicija VE-PTP poveča VP, skladno z njegovim učinkom na defosforilacijo VE-kadherina [19,24] . Poleg tega VE-PTP defosforilira VEGFR2 na način, odvisen od Ang1/Tie2-, kar zavira fosforilacijo VE-kadherina [25]. Po drugi strani pa se med VEGF stimulacijo ekstravazacije levkocitov VE-PTP disociira od VE-kadherina, da se odpre AJ [26]. Skratka, VE-PTP regulira VP s svojim kombiniranim delovanjem na defosforilacijo VE-kadherina, supresijo Tie2 in regulacijo VEGFR2. Hkratno ciljanje na VEGF, Angpt2 in VE-PTP bi lahko bile obetavne terapevtske strategije za mikroangiopatijo [27].
Podobno kot pri raziskavah o VEGF so ti podatki pridobljeni predvsem iz mišjih modelov [19-21,23,27], človeških EC linij [19,21,23,27] in mišjih EC linij [21, { {9}}], ki prikazuje učinke signala Angpt/Tie preko transcelularne [21] in paracelularne [19,20,24,25]poti. Klinično preskušanje [22] zagotavlja dokaze o tem, kako Angpt2 modulira VP prek poškodbe glikokaliksa pri bolnikih, in potrebnih je več kliničnih študij za povečanje zanesljivosti trenutnih zaključkov.

Semaforin razreda 3 in NRP1
Semaforini razreda 3 so izločene topne molekule, ki so bile prvotno identificirane kot aksonski vodilni proteini. NPL je v membrani zasidran receptor za semaforine razreda 3 pri vretenčarjih, ki lahko nekonkurenčno vežejo VEGF in sprožijo ustrezne poti navzdol [28].
NRP1 kot koreceptor VEGF/VEGFR2 lahko poveča afiniteto ligand-receptor in sodeluje pri prenosu signala [11,28]. Poleg tega lahko NRP1 in VEGFR2 posredujeta VP neodvisno drug od drugega [29]. Na primer, pot SEMA3A/NRPl zavira aktivnost PP2A prek signala Src/Set, ki vodi do fosforilacije VE-kadherina pri serinu S665 in internalizacije ali sproži pot PI3K/Akt [30, 31]. Prav tako lahko SEMA3A sodeluje s kompleksom VEGFR1/NRP2, da izzove aktivacijo Mical2, dezorganizacijo F-aktina in motnje citosol-Etona [32]. Poleg tega je naša preiskava identificirala SEMA3Cas kot pro-prepustni dejavnik, ki prispeva k poškodbi tkiva med AKI. Zanimivo je, da je SEMA3A anti-angiogen in do neke mere nasprotuje VEGF-A, medtem ko spodbuja VP [31]; Funkcije SEMA3C so podobne VEGF, saj spodbuja angiogenezo in VP pri miših (Cai A et al, podatki v reviziji). Ti rezultati kažejo, da lahko pot SEMA3A (SEMA3C)/NRP1 sodeluje pri različnih boleznih z modulacijo VP, ki ne vključuje le same poti, temveč tudi njeno interakcijo z VEGFR. Kar zadeva možno terapijo, lahko posebej inhibiramo mesto vezave semaforina razreda 3 na NRP1, da blokiramo odziv prepustnosti, medtem ko ostane vezava VEGF nedotaknjena, da se ohrani proliferacija in preživetje EC.
Skupaj je vir teh podatkov kombinacija poskusov in vivo z mišjimi modeli [28-32] in celične kulture in vitro z uporabo človeških EC linij [29-31] ali mišjih linij [32]. Predlagano je, da se semaforini razreda 3 vežejo na NRP1, da inducirajo VP preko paracelularne poti, toda kako ga prevesti v klinično prakso, je potrebna nadaljnja raziskava.
Vnetni dejavniki in ekstravazacija levkocitov. Vaskularna hiperpermeabilnost, ki jo povzročajo različni vnetni dejavniki, ima ključno vlogo pri vnetju in anafilaksiji. Histamin, pomemben vnetni dejavnik, ima 4 sorodne receptorje, povezane z G proteinom, imenovane HIR do H4R. Histamin poveča VP prek HIR, ki ga lahko aktivira tudi faktor aktivacije trombocitov (PAF). Aktivacija H1R spodbuja mobilizacijo kalcija, posredovano s PLC, in pot RhoA/ROCK, ki skupaj inducirata fosforilacijo lahke verige miozina in prerazporeditev VE-kadherina, sledi nastanek vrzeli [33]. Poleg zgoraj omenjene poti eNOS, ki vključuje hemodinamske spremembe in z NO inducirano S-nitrozilacijo -katenina, p120 in VE-kadherina, predstavljajo še en pomemben pro-prepustni mehanizem teh vnetnih dejavnikov [34, 35]. Poleg tega TNF-a, še en znan provnetni citokin, močno spodbuja prepustnost s sprožitvijo signala RhoA/ROCK, aktiviranjem poti Rac/ROS za ločitev VE-PTP od VE-kadherina in moduliranjem molekul TJ, vključno z ZO{ {21}}, okludin in klavdin [36, 37].
Ekstravazacija levkocitov, ključni dogodek pri vnetju, je tesno povezana z VP prek VE-kadherina, saj je antipermeabilnost prek kompleksa VE-kadherin-a-katenin močno zmanjšala infiltracijo levkocitov v določenih tkivih, ne da bi vplivala na signal VEGFR2, VE-PTP združenje ali citoskeletna organizacija [13, 38]. Zanimivo je, da ekstravazacijo VP in levkocitov uravnavajo različni tirozini VE-kadherina, saj fosforilacija pri Y685 omogoča ekstravazacijo VP in levkocitov, defosforilira Y731 [39]. Ne glede na to, da VE-PTP deluje selektivno na Y685, je ključnega pomena pri transmigraciji levkocitov, ker stimulacija VEGF ali vezava limfocitov na adhezijsko molekulo vaskularnih celic-1 aktivira pot Race/NOX/ROS/Pyk2, ki posreduje pri ločitvi VE-PTP od VE-kadherin, potreben za VP in diapedezo levkocitov in vivo [26]. Poleg tega fosforilacija VE-kadherina Y685 podpira difuzijo kemokinov iz vnetega intersticija v vaskularni lumen, s čimer spodbuja povratno transendotelijsko migracijo aktiviranih nevtrofilcev, da povzroči poškodbe oddaljenih organov [40].
Vse te predklinične raziskovalne študije o vnetnih citokinih in celicah temeljijo na mišjih modelih [33-40] s pomočjo človeških linij EC [33,35,38,39] ali izoliranih primarnih celic [36, 39]. Skupaj imajo ti vnetni dejavniki več skupnih mehanizmov ne le med samimi, temveč tudi angiogenimi dejavniki, in zdi se, da ima modifikacija VE-kadherina za olajšanje paracelularne poti osrednjo vlogo. Poti, ki uravnavajo VP, so povzete na sliki 2.

Slika 2. Glavne signalne poti, ki uravnavajo VP. Te poti vključujejo predvsem angiogeno signalno pot (VEGF/VEGFR2, Angpt/Tie2 in SEMA3A/NRP1) in vnetno signalno pot (histamin/HIR, PAF/PAFR, TNF-a/TNFR in levkociti/VCAM{{6} }). Ne glede na natančen proces signalne transdukcije modulirajo skupni substrat, VE-kadherin, v AJ. Fosforilacija VE-kadherina pri Y658, Y685 in S665 vodi do internalizacije, ki ji sledi razgradnja ali recikliranje, s čimer se poveča VP. VE-PTP zavira fosforilacijo VE-kadherina in VEGFR2 za stabilizacijo endotelijskih stikov; zato njegova disociacija od VE-kadherina poveča VP.S-nitrozil-delovanje VE-kadherina, -katenina in pl20 posreduje pri motnjah AJ in endocitoze VE-kadherina. Fosforilacija MLC, stresnega vlakna, spodbuja preureditev in prerazporeditev VE-kadherina, da se odpre endotelijski stik. Levkociti defosforilirajo VE-kadherin Y731, da povzročijo ekstravazacijo. VP modulirajo tudi TJ, ekspresija caveolina-l (transcelularni transport), odstop pericita in hemodinamični dejavniki. VP, žilna prepustnost; VE-kadherin, vaskularni endotelijski kadherin; AJ, adherentni spoj; VE-PTP, vaskularni endotelijski protein tirozin fosfataza; MLC, lahka veriga miozina; TJ, tesna stičišča; IS, indoksil sulfat; EC, endotelna celica.
