Kombinirana pangenomika in transkriptomika razkriva jedro in redundantne virulentne procese v hitro razvijajočem se glivičnem rastlinskem patogenu
Dec 05, 2023
Povzetek
Ozadje
Preučevanje genomskih variacij pri hitro razvijajočih se patogenih potencialno omogoča identifikacijo genov, ki podpirajo njihovo "jedrno biologijo", saj so prisotni, funkcionalni in jih izražajo vsi sevi ali "fleksibilna biologija", ki se razlikuje med sevi. Geni, ki podpirajo prožno biologijo, se lahko štejejo za "pripomočke", medtem ko je "jedrni" nabor genov verjetno pomemben za skupne značilnosti biologije patogene vrste, vključno z virulenco na vseh genotipih gostiteljev. Pšenično patogena gliva Zymoseptoria tritici predstavlja eno najhitreje razvijajočih se groženj svetovni prehranski varnosti in je bila v središču te študije.

koristi cistanche za moške - krepitev imunskega sistema
Kliknite tukaj za ogled izdelkov Cistanche Enhance Imunity
【Vprašajte za več】 E-pošta:cindy.xue@wecistanche.com/Whats App: 0086 18599088692/Wechat: 18599088692
Rezultati
Konstruirali smo pangenom 18 evropskih terenskih izolatov, pri čemer je bilo 12 med okužbo izpostavljenih tudi profiliranju transkripcije RNAseq. Z združevanjem teh podatkov smo predvideli "jedrni" genski niz, ki obsega 9807 sekvenc, ki so bile (1) prisotne v vseh izolatih, (2) brez inaktivacijskih polimorfizmov in (3) izražene v vseh izolati. Določen je bil tudi velik dodatni genom, ki ga sestavlja 45 % vseh genov. Genetski in genomski polimorfizem smo razvrstili tako na kromosomsko kot individualno gensko lestvico. Beljakovine, potrebne za bistvene funkcije, vključno z virulentnostjo, so imele nižjo od povprečne variabilnosti zaporedja med osnovnimi geni. Tako jedrni kot dodatni genomi so kodirali veliko majhnih, izločenih kandidatnih efektorskih proteinov, ki verjetno vplivajo na imunost rastlin. Z virusnim vektorjem posredovano prehodno stanje v plantažni prekomerni ekspresiji 88 kandidatov ni uspelo identificirati nobenega, ki je povzročil nekrozo listov, značilno za bolezen. Vendar pa je funkcionalna komplementacija nepatogenega delecijskega mutanta brez petih jedrnih genov pokazala, da je bila popolna virulenca obnovljena s ponovno uvedbo enega samega gena, ki kaže najmanj polimorfizem zaporedja in največjo ekspresijo.
Sklepi
Ti podatki podpirajo kombinirano uporabo pangenomike in transkriptomike za definiranje genov, ki predstavljajo jedro in potencialno izkoriščene slabosti pri hitro razvijajočih se patogenih.
Ključne besede
Mozaični virus lisičjega repa, Septoria tritici, nekrotrofni efektor, esencialni geni, pomožni kromosomi, dotideomicete,Kromosomska nestabilnost, Mycosphaerella spp
Ozadje
Trajnostni nadzor nad nalezljivimi boleznimi, ki prizadenejo živali in rastline, je izziv zaradi razvoja mikroorganizmov, ki jih povzročajo [1, 2]. Bolezni, ki jih je najtežje nadzorovati, so tiste, ki jih povzročajo najhitreje razvijajoče se vrste, ki se lahko hitro odzovejo na selektivne pritiske, vključno z naravno imunostjo gostitelja, neugodnimi okoljskimi razmerami in/ali protiinfektivnimi zdravili [1, 3]. Možnost hitrega razvoja mikrobnih patogenov določa več značilnosti, med drugim; (1) hiter življenjski cikel in (2) mehanizmi, ki spodbujajo spolno razmnoževanje [4]. Slednje lahko privede do velikih stopenj stalnih genetskih variacij, ki obstajajo znotraj populacij patogenov, ki se lahko ohranijo in povečajo ob zunanjih selektivnih pritiskih. Medtem ko je verjetno, da bodo določeni geni izkazovali naravne variacije genetskega zaporedja, ki poganjajo njihov razvoj, drugih ni mogoče izgubiti (ali inaktivirati z mutacijo), ne da bi to vplivalo na sposobnost patogenov. Pri evkariontskih in prokariontskih rastlinskih patogenih je ta razlika v ravneh polimorfizmov med geni privedla do realizacije "genomov dveh hitrosti" [5], ki obsegajo nekatere komponente, ki se hitro razvijajo in naj bi se odzivale na zunanje dejavnike (razpon gostiteljev in imunost itd.), medtem ko počasneje razvijajoči se niz vsebuje gene z glavnimi gospodinjskimi in drugimi bistvenimi funkcijami. Dodatni in jedrni deli genomov patogenov se lahko sestavijo v "pangenom", ki naj bi predstavljal skoraj celoten nabor genov, prisotnih v vrsti [6]. Velikost jedra in pomožnih delov pangenomov se razlikuje glede na vrsto bakterij, gliv in oomicet [7–13] in lahko kaže na možnost, da se mikrobne populacije hitro razvijejo do selektivnih pritiskov. Možno je, da večji kot je dodatni pangenom glede na jedro, bolj so te populacije sposobne za hiter razvoj. Askomicetni glivični patogen pšenice, Zymoseptoria tritici, je povzročitelj pegavosti Septoria tritici (STB), svetovno pomembne bolezni, ki ogroža prehransko varnost [14]. Patogen je dolgo veljal tudi za modelni sistem za študije populacijske biologije in evolucije [15–18]. To je zato, ker ima Z. tritici visoko stopnjo spolne rekombinacije, ki ohranja velike količine stalne genetske raznolikosti v svojih populacijah in omogoča hitro prilagajanje na globalni in lokalni ravni [17, 19–24]. Posledično so glavni geni pšenice, ki dajejo odpornost na Z. tritici, hitro premagani [25]. Poleg tega večina široko uporabljenih komercialnih fungicidov sčasoma izgubi svojo učinkovitost [3]. Kombinacija teh dveh dejavnikov predstavlja grožnjo svetovni proizvodnji pšenice, ki jo je treba nujno obravnavati. Z. tritici se je nedavno pojavil tudi kot nov model za genomiko patogenov s številnimi visokokakovostnimi referencami genoma, ki so zdaj na voljo [26] poleg pangenomov, zgrajenih iz velikega števila posameznih izolatov genomov [27, 28]. Morda je ena najzanimivejših značilnosti genoma Z. tritici prisotnost 13 jedrnih kromosomov (1-13), ki jih najdemo v vseh izolatih, nato pa do nadaljnjih 8 manjših pomožnih kromosomov (14-21), ki kažejo prisotnost/odsotnost in strukturni polimorfizem med izolati [26, 29]. Na srečo ima eden od referenčnih izolatov skupnosti in prvi, ki je bil popolnoma sekvenciran, nizozemski terenski izolat IPO323, zbran v osemdesetih letih prejšnjega stoletja, 21 kromosomov, kar je največje število, opaženo do danes. Zato IPO323 služi kot odlično merilo za preučevanje variacij v drugih izolatih in kot ogrodje za gradnjo pangenomov.

cistanche tubulosa - izboljšanje imunskega sistema
Cikel nespolne okužbe z Z. tritici je značilen za številne sorodne rastlinske patogene, ki prizadenejo številne živilske pridelke [30]. Te glive, ki pripadajo družini Mycosphaerellaceae iz reda Dothideomycetes, običajno vdrejo v rastlinska tkiva skozi želodce [30, 31]. Nato sledi obdobje dolge asimptomatske rasti med rastlinskimi celicami, ki traja vsaj 8 dni in se nenadoma konča z nastankom nekrotičnih lezij na listih, kar je za Z. tritici očitno posledica "hiperaktivacije" rastline. imunost [32–34]. Smrt rastlinske celice je nato povezana s tvorbo novih sporulacijskih struktur, piknidijev, v substomatalnih votlinah ter kasnejšim iztiskanjem in širjenjem novonastalih piknidiospor v obdobjih pljuskajočega dežja. Za druge glive Dothideomycetes je bilo dokazano, da izzovejo hiperaktivacijo rastlinske imunosti z izločanjem beljakovinskih "efektorjev", ki jih prepoznajo občutljive rastline, kar povzroči smrt celic in tkiv (nekroza ali programirana celična smrt). Te nekrotrofne glive imajo koristi od tega odziva in vključeni efektorski proteini se zdaj imenujejo nekrotrofni efektorji [35, 36]. Medtem ko obstaja nekaj predhodnih dokazov, da bi Z. tritici lahko uporabil tudi nekrotrofne efektorje pri prehodu na simptomatsko rast [37], kar bi povzročilo poškodbe listov, ta hipoteza do danes ni bila trdno preizkušena. Dve medsebojno neizključujoči poti za zaščito prihodnje proizvodnje pšenice pred vplivom STB sta (1) povečanje naravne odpornosti rastlin na bolezni in (2) prepoznavanje novih molekularnih tarč, ki bi jih lahko izkoristili za nadzor bolezni. V idealnem primeru bi ti omogočili selektivni nadzor patogena, medtem ko bi druge okoljske in ekološke vplive omejili na minimum. Genomika patogenov in zlasti pangenomika nudita potencial za povečanje obeh strategij. Medtem ko lahko proteini, ki jih kodira pomožni, hitro razvijajoči se del pangenoma, vsebujejo veliko genov, ki medsebojno delujejo z imunostjo rastlin (npr. efektorji), lahko osrednji genom predstavlja tarče, ki manj hitro mutirajo zaradi negativnih kazni glede sposobnosti (in virulence). Iz tega razloga kmetijski fungicidi običajno ciljajo na osnovne procese, ki verjetno veljajo za manj spremenljive. Vendar, kot je bilo že omenjeno, se lahko celo te tarče do neke mere razvijejo, da se izognejo kemični inhibiciji, kot je opisano za številne trenutne tarčne proteine fungicidov [3, 14]. Večina fungicidov, ki so bili doslej uporabljeni, je ciljala na precej ozek nabor molekularnih procesov (npr. biosinteza sterola, dihanje itd.) [3]. Obstaja potencialno veliko drugih tarč, ki bi jih lahko uporabili za selektivno kontrolo glivičnih patogenov, ki bi morali nastati pri združevanju in analizi več podatkovnih nizov omics. Velik potencial za odkritje je poudarjen z dejstvom, da je običajno do 40 % vseh genov, identificiranih v zaporedjih genoma patogenih gliv (in gliv na splošno), še vedno neznane funkcije. Tisti, ki so prisotni in morda ohranjeni v jedru genoma patogenih gliv, so lahko še posebej pomembni.
Pangenomics of rapidly evolving pathogens could be used to identify core, potentially specific gene sets, which could be exploited in future disease control [11]. The premise is that genes which are not evolving, in an otherwise rapidly evolving species, are most likely to be essential for either life or important for key virulence processes of the pathogen. Pangenomes themselves have, to date, largely been defined by sequencing genomic DNA from multiple members of a species. Whilst this is a critical and indispensable step in ascertaining the full potential of a species' genomics, gene expression support is perhaps overlooked for refinement of core and accessory gene calls, particularly in relation to biological processes such as pathogenicity/virulence. For example, if a core gene, predicted through genomic DNA sequence analysis, is not expressed by a successful pathogenic strain/ isolate during infection, it might be more appropriately considered accessory. Pangenome analyses on fungi and yeasts have recently emerged and have highlighted some major differences in the size of core and accessory gene components. For example, one recent study which analyzed the animal pathogenic yeasts, Candida albicans, Cryptococcus neoformans, the free-living yeast, Saccharomyces cerevisiae, and the animal filamentous fungal pathogen Aspergillus fumigatus, predicted each to have >80 % genov označenih kot jedro [10]. Vendar pa so druge analize z rastlinami povezanih gliv plamenk napovedale večje dodatne genske komponente, vključno s ~38 % za patogene Claviceps purpurea [38] in ~44 % za Pyrenophora tritici-repentis [39]. Prejšnje obsežne pangenomske študije o Z. tritici so uporabljale globalne in zgodovinske populacije, ki so vključevale veliko število izolatov, ki so bili sekvencirani na lestvicah fragmentiranega in celotnega genoma [27, 28]. Te študije so identificirale velik nabor pomožnih genov (~40 % vseh genov) za to vrsto. Poleg tega je bilo to povezano z obsežno prisotnostjo/odsotnostjo in kromosomskimi strukturnimi polimorfizmi, kar je vključevalo tudi dinamične ponavljajoče se elemente (vključno s prenosljivimi elementi). Nadaljnja analiza je tudi pokazala, da so številni dodatni geni tudi nižje izraženi (v povprečju) kot jedrni geni. Te študije predstavljajo "zlati standard" za strukturo pangenoma vrste Z. tritici in najobsežnejše doslej za katero koli nitasto glivo. Vendar ostaja vprašanje za to in druge vrste, v kolikšni meri bi se lahko pangenomika uporabila za identifikacijo osnovnih genov in procesov virulence. Ali znotraj osrednjih genskih nizov, ali ravni polimorfizmov celotne populacije, ki vplivajo na spremembe aminokislin, kot tudi ravni izražanja genov, izdajo identiteto ključnih genov virulence patogenov?
V tej študiji smo združili sekvenciranje genoma in transkriptomske pristope na osnovi RNAseq, da smo izdelali pangenom iz nedavne evropske zbirke izolatov Z. tritici. Naš glavni cilj je bil preizkusiti, ali imajo geni, prisotni v jedru genoma, ki kodirajo proteine z nizkimi stopnjami polimorfizma aminokislin (tj. v kodirnih sekvencah) med izolati, pomembne funkcije, vključno z glavnimi vlogami v procesih okužbe jedra na pšenici. V skladu s prejšnjimi študijami [27, 28] dokazujemo, da ima Z. tritici izjemno velik dodatni genom (~45 % vseh genov), ki podpira njegov hitro razvijajoči se status. Poleg tega nudimo biološke podatke, ki jasno podpirajo uporabnost kombinirane uporabe obeh metod omics za identifikacijo novih genov jedra virulence. Nasprotno pa visoko zmogljivi zasloni za čezmerno ekspresijo funkcionalnih beljakovin, posredovani z virusi, niso uspeli identificirati nobenih kandidatov za nekrotrofne efektorje, ki so odgovorni za izzivanje bolezenskih lezij v listih pšenice, bodisi iz jedra ali pomožnega pangenoma.

rastlina cistanche krepi imunski sistem
Rezultati
Preverjanje virulence v evropski zbirki Z. tritici identificira podobno agresivne seve z geografsko nepovezanih lokacij
Preizkusili smo virulenco 43 izolatov Z. tritici na 21 široko občutljivih evropskih sortah krušne pšenice, da smo skupaj pridobili 2709 podatkovnih točk (vključno s tremi ponovitvami). Informacije o izolatu (koda in država izvora) so predstavljene v Dodatni datoteki 1: Tabela S1. Vsako interakcijo smo kvantitativno ocenili za naslednje parametre: (1) dolžino inkubacijske dobe, (2) čas, potreben za dosego popolne nekroze (ko se je pojavila) in (3) ravni nespolne sporulacije (slika 1A). Na podlagi računalniškega in vizualnega točkovanja bolezni (glejte metode in dodatno datoteko 2: slika S1) so bili vsi izolati nato razvrščeni glede na njihove profile virulence na testirani plošči kultivarja (slika 1B). Izolat pozitivne kontrole IPO323, ki služi kot globalna referenca [26] s popolnoma sekvenciranim genomom, je bil manj agresiven od večine testiranih izolatov proti skoraj vsem kultivarjem. Ta izolat je bil zbran leta ~1984 in je bil od takrat shranjen v skladišču z občasnim ponovnim prehodom skozi liste pšenice; zato trenutno ni jasno, ali bi to opažanje lahko (vsaj delno) izhajalo iz shranjevanja vzorcev skozi čas. Identificirali smo sedem izolatov, ki niso mogli povzročiti simptomov bolezni na nobeni od sort pšenice (slika 1B). Ker vsi ti izolati izvirajo iz Španije ali Italije, kjer pogosteje gojijo tetraploidno (trdo/testeninsko) pšenico (Triticum durum L.), je verjetno, da so bili ti izolati specifični za trdo pšenico [40, 41]. Pomembno je, da se izolati s podobnimi virulenčnimi profili niso združili na svojih lokacijah zbiranja, pri čemer so bili izolati, ki izvirajo od daleč na vzhodu kot Slovaška do daleč na zahodu kot Irska, vsi združeni (slika 1B). Ta ugotovitev se dobro ujema z visokimi stopnjami genetskih variacij, ki obstajajo med izolati in prejšnjimi študijami, ki so pokazale, da je to enako visoko na lestvici lezije posameznega lista pšenice kot po celinah [42]. Veliko bolj agresivnih izolatov z izrazitimi virulenčnimi profili je bilo nato izbranih za genomsko sekvenciranje (označeno z "#" na sliki 1B) in analizo RNAseq (označeno z "+" na sliki 1B).
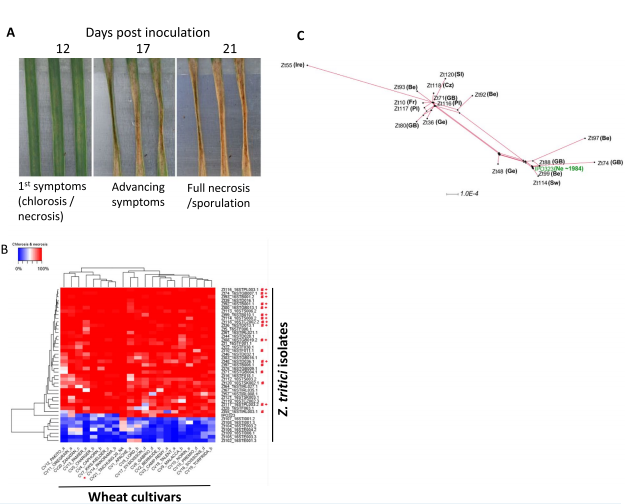
Slika 1 Ocene virulence evropske zbirke izolatov proti vrsti heksaploidnih (krušnih) sort pšenice. Tipičen časovni potek napredovanja bolezni, ki ponazarja parametre, ocenjene na zaslonu, vključno s časom, potrebnim do pojava prvih vidnih simptomov in do pojava popolne nekroze listov na inokuliranem območju. Slika prikazuje okužbo pšenice sorte Riband z izolatom Z. tritici IPO323. B Profil virulence izolatov v primerjavi s ploščo kultivarja na podlagi stopenj nekroze in kloroze listov. Meritve so bile opravljene tako z vizualnimi ocenami kot z uporabo programske opreme za analizo slik LemnaTec in LemnaGrid s primerljivimi končnimi rezultati. Izolati so bili razvrščeni in razvrščeni v skupine na podlagi podatkov o virulentnosti. Izolati Z. tritici, označeni z #, so bili genomsko sekvencirani za izdelavo pangenoma. Izolati, označeni z +, so bili analizirani tudi s transkriptomiko RNAseq. Za sorto pšenice Panorama (označeno z X) je bilo ugotovljeno, da je enako in popolnoma dovzetna za večino izolatov in je bila izbrana kot gostiteljski genotip za okužbo listov RNAseq. Upoštevajte, da so podatki o nizki virulenci za zunanjo skupino sedmih izolatov proti vsem kultivarjem verjetno posledica tega, da so ti izolati prilagojeni za povzročanje bolezni na tetraploidni pšenici (Durum ali Pasta). Vsi podatki so reprezentativni za tri okužene liste, analizirane/medsebojno z njimi iz dveh poskusov biološke ponovitve (skupaj 6 listov). C SplitsTree analiza molekularne filogenije izolatov, izbranih za genomsko sekvenciranje. Država izvora izolatov je prikazana v okrajšavi (Pl=Poljska; GB=Velika Britanija; Be=Belgija; Cz=Češka; Ge {{8 }} Nemčija; Sw=Švedska; Fr=Francija; Sl=Slovaška; Ir=Irska). Predstavljen je tudi referenčni izolat IPO323, zbran ~1984 na Nizozemskem (Ne).
Zaporedje genoma in filogenetska analiza na sedemnajstih evropskih izolatih razkrivata visoko stopnjo genske raznolikosti
We used Illumina HiSeq 250 bp paired-end read technology to assemble the gene space of seventeen new isolates (indicated by # in Fig. 1B). BUSCO analysis (core dataset Pezizomycotina) was then performed to assess the completeness of each genome assembly (Table 1). Scores >97 % v vseh primerih je pokazalo dobro sestavo genskega prostora (kodirajoče regije) za vse izolate. Nekaj izbranih genov BUSCO je manjkalo v vseh sklopih, kar kaže na to, da Z. tritici morda nima ortologov teh genov. Da bi določili količino genetske variacije, ki vpliva na predvidene kodirne regije, smo nato izvedli analizo SNPEf za vsak sev proti pangenomu, zgrajenemu na celotnem genomu referenčnega izolata IPO323 (tabela 2). Ta analiza je pokazala, da je imel vsak nov sev več kot 160000 SNP-jev proti izpeljanemu pangenomu. Med temi je bilo več kot 65, 000 ki so povzročili morebitno izgubo delovanja beljakovin (močan učinek, premik okvirja, izgubljeni začetek, prezgodnji stop kodoni) ali sprožili spremembo aminokislin v predvidenih beljakovinah (zmerno). Ti podatki so pokazali gensko raznolikost, ki obstaja med izolati Z. tritici.
Analiza razdeljenega drevesa je bila izvedena na 17 na novo sekvenciranih sevih in IPO323, da bi ugotovili, ali so izolati s podobnimi vzorci okužbe kultivarjev imeli kakšno filogenetsko povezavo in ali je bilo to povezano z državo izvora. Filogenija je bila določena z uporabo veriženja šestih kodirnih in nekodirajočih zaporedij (glejte metode in dodatno datoteko 3: podatki S1). Drevo (slika 1C) še enkrat ponazarja, da ni bilo jasne povezave med profili virulence in mestom vzorčenja za sekvencirane izolate, pri čemer so tesno povezani profili virulence (v primerjavi s sliko 1B) vidni pri izolatih, zbranih iz različnih evropskih držav, ki so bili kljub temu filogenetsko tesno povezani.
Konstrukcija in analiza pangenoma napovedujeta 9807 "jedrnih" in 8083 "dodatnih" genov
Poleg zaporedij genoma smo izbrali 12 izolatov za profiliranje transkripcije na osnovi RNAseq (označeno z + na sliki 1B). Vsak izolat je bil profiliran v treh izvodih med aksenično rastjo v brozgi YPD in tudi na dveh neodvisnih stopnjah okužbe listov; 6 dni po inokulaciji (dpi), kar predstavlja srednjo fazo brez simptomov, in 9 dpi, v prehodni fazi zgodnjega razvoja simptomov. Univerzalno občutljiva sorta pšenice Panorama je bila uporabljena za teste okužbe, ki so jo vsi izolati lahko popolnoma okužili z nerazločno kinetiko. Z uporabo teh podatkov transkriptoma v kombinaciji z novimi sklopi genoma in izvirnega referenčnega zaporedja IPO323 kot ogrodja smo določili pangenom za evropske izolate, ki vključuje tudi zaporedja, prisotna v drugih izolatih, ki niso bili odkriti v IPO323. Koraki v konstrukciji pangenoma in naša merila za kategorizacijo genov kot "jedro" ali "pripomoček" so prikazani na sliki 2. Pomembno je, da polimorfizem zaporedja inaktivacije (visok učinek, izguba funkcije-LoF) ter prisotnost in odsotnost, premisleki so bili podprti tudi z dokazi o izražanju genov. Zato mora biti gen prisoten v funkcionalni obliki in izražen z vsemi izolati, da se uvrsti v kategorijo "jedro". Naš splošni pristop (slika 2) je opredelil skupni pangenom 17.890 genov, vključno z 2017, ki niso bili prisotni v IPO323. Naslednji koraki filtriranja so 9807 kategorizirali tako, da se nahaja v jedrnem genomu, z le nekoliko manjšim številom, 8083, v kompletu dodatne opreme. Slednji predstavlja približno 45 % celotnega pangenoma, kar je rahlo povečanje glede na prej opisano [28]. Čeprav se te številke na splošno dobro ujemajo, so ocene pomožnih genov bolj subjektivne glede pristranskosti zaradi uporabljenih metod (Panseq itd.) in ne moremo domnevati, da dodatna prihodnja analiza morda ne bo zmanjšala števila pomožnih genov z uporabo, na primer, ortološkega pristopi. Vse pangene so analizirali glede na več značilnosti (napovedi izločanja, povezanost z membrano, lokalizacijo in vsebnost cisteina) in predvidene funkcije (opombe BLAST, GO in Interpro). Na voljo je tabela z vsemi razpoložljivimi informacijami o vseh genih (dodatna datoteka 4: tabela S2). Tabela prikazuje tudi relativne srednje ravni genske ekspresije, pridobljene z RNAseq, določene za vse gene za vseh 12 izolatov pod tremi testiranimi pogoji. Če skupaj primerjamo tudi s prejšnjimi pangenomskimi študijami o tem organizmu [27, 28], je jasno, da ima Z. tritici eno od največjih števil pomožnih genetskih komponent gliv, ki so bile doslej raziskane, kar verjetno odraža njen hiter razvoj narave.
Tabela 1 BUSCO analiza novih genomov

Tabela 2 Povzetek učinkov SNP za vsak nov genom v primerjavi z referenčnimi genskimi modeli IPO323


Slika 2 Povzetek korakov, uporabljenih za ustvarjanje "jedrnih" in "pomožnih" genskih klicev in številk za novo zgrajen evropski pangenom Z. tritici. Številke predstavljajo število genov, identificiranih v vsaki fazi nastajanja
Strukturne značilnosti variacije v evropskem pangenomu Z. tritici
Cilj te študije je bil preizkusiti hipotezo, da bi lahko pangenomiko izkoristili za identifikacijo pomembnih novih genov, bodisi bistvenih za življenje ali za virulenco v patogenih organizmih. Domnevali smo, da bi bili to geni, ki so prisotni in funkcionalni v vsakem sevu patogena ter se izražajo v njem. Nadalje smo špekulirali, da bi ti geni imeli nižje ravni mutacij SNP z visokim in zmernim učinkom, ki vplivajo na kodirne sekvence (manj polimorfne) in da se lahko združujejo v regijah na določenih kromosomih.
Uporabili smo podatke o variacijah SNP (visoko, zmerno in modifikator – glejte dodatno datoteko 4: Tabela S2), kot tudi podatke o povprečni ekspresiji za vse gene, da bi raziskali povprečne ravni kodirajočega polimorfizma in ekspresije na kromosomski osnovi z uporabo 21 kromosomov IPO323 kot oder. Modifikatorji SNP predstavljajo spremembe nukleotidov, ki ne sprožijo spremembe aminokislin. Slika 3A prikazuje, da ni bilo posebne pristranskosti za frekvenco mutacije, ko so bili kumulativni visoki, zmerni in modifikatorski SNP izraženi kot značilnost povprečne dolžine beljakovin na celoten kromosom. Ko pa smo izpustili modifikatorske mutacije, tj. tiste, ki ne povzročijo spremembe aminokislin, je bilo jasno, da ima najmanjših 8 kromosomov gene z večjim številom visokih in zmernih mutacij SNP (slika 3B). Ta učinek je bil dodatno poudarjen, ko so bili analizirani samo SNP z visokim učinkom (slika 3C). V nasprotju z ravnmi, očitnimi na jedrnih kromosomih 1–13 (~20 %), je bilo do 90 % genov, ki se nahajajo na osmih najmanjših kromosomih 14–21, podvrženih močnemu učinku, verjetno mutacijam zaradi izgube funkcije v vsaj enem izolat (slika 3C). Podatki o kumulativni transkripciji iz vseh 12 novih izolatov so prav tako pokazali relativno nizko povprečno izražanje genov, prisotnih na kromosomih 14–21 (slika 3D), kot je bilo prej opaženo za IPO323 [32, 43, 44]. Skupaj ti podatki kažejo na jasno genomsko razdelitev, z najmanjšimi osmimi dodatnimi kromosomi, ki vsebujejo zaporedja, ki so zelo polimorfna, dodatna in na splošno slabo izražena.
Primerjava vseh genov v jedrnem ali dodatnem genomu je pokazala, da je bilo približno 60 % vseh genov v slednjem najdenih v vsaj enem sevu z mutacijo z visokim učinkom (izguba funkcije (LoF)) in da jih je bilo 47 % prav tako odsotnih pri vsaj en sev (dodatna datoteka 4: tabela S2). Podobno kot pri analizi pomožnih kromosomov so bili tudi posamezni pomožni geni na splošno zelo slabo izraženi v testiranih izolatih (dodatna datoteka 4: tabela S2) in so imeli veliko večje število zaporedij z neznanimi funkcijami (približno 80 %). Ta opažanja se dobro primerjajo s prejšnjimi pangenomskimi študijami, izvedenimi na globalnih zbirkah Z. tritici, zbranih desetletja narazen [27, 28].
Izvedli smo tudi analizo variacije prisotnosti in odsotnosti genov (PAV) za vse gene, predvidene v referenčnem izolatu IPO323, za ostalih 17 sekvenciranih izolatov. Ti podatki o prisotnosti/odsotnosti so bili narisani položajno za vsak gen na vsakem od 21 kromosomov, prisotnih v IPO323. Sliki 3E in F prikazujeta podatke iz reprezentativnih jedrnih kromosomov (1 in 7), medtem ko sliki 3G in H prikazujeta podatke za reprezentativna pomožna kromosoma (13 in 14). Podatki za preostale kromosome so prikazani v dodatni datoteki 2: slika S2. Ta analiza je identificirala veliko genov, prisotnih v IPO323, ki manjkajo v številnih ponovno sekvenciranih izolatih, in jasno kaže razliko v splošni prisotnosti/odsotnosti genov med "jedrnimi" kromosomi IPO323 (ki jih najdemo v vsakem sevu Z. tritici) v primerjavi z 8 najmanjšimi "pomožnimi" kromosomi. Podatki poudarjajo tudi regijo na kromosomu 7, zlasti med 1,7 Mb in 2,5 Mb, ki kaže visoko frekvenco odsotnosti genov v novih izolatih (slika 3F). Zanimivo je, da se ta regija natančno ujema z lokacijo genoma, za katero je bilo prej ugotovljeno, da ima minimalno ali nič genske ekspresije v IPO323 bodisi med rastjo v kulturi ali med katero koli fazo okužbe rastlin [32, 43]. Ta regija se ujema tudi s kromosomsko delecijo, ki so jo opazili pri jemenskem izolatu v prejšnji študiji pangenoma [28]. Ti podatki skupaj krepijo idejo, da Z. tritici predstavlja hitro razvijajoč se organizem z visokimi ravnmi in različnimi tipi genetske in genomske raznolikosti znotraj svoje populacije.
Napovedi lokalizacije beljakovin razkrivajo gene v dodatnem pangenomu, ki lahko delujejo pri prilagajanju spreminjajočim se okoljem
Napovedi lokalizacije beljakovin WolfPsort so bile izvedene na vseh proteinih, ki jih kodira pangenom. Nato smo izračunali relativni odstotek beljakovin, za katere je bilo predvideno, da se bodo lokalizirale v vsako subcelično regijo kot značilnost skupnega števila beljakovin za jedro ali dodatni pangenom (slika 4). V jedrnem genomu je bilo obogatenih več kategorij lokalizacije, vključno s "citoplazmo", "zunajcelično" in "plazemsko membrano", od katerih slednja vsebuje številne ključne transportne funkcije (slika 4). Nasprotno, lokaciji "jedro" in "mitohondriji" sta bili povezani z višjim odstotkom genov v dodatnem genomu (slika 4). Dodatni genom je bil obogaten za posebne domene, ki vežejo cink, kar lahko zagotovi transkripcijsko prožnost. O obogatitvi te kategorije so poročali tudi v prejšnji študiji pangenoma, ki je poudarila, da je naš celoten cevovod ustvaril primerljive rezultate [27, 28]. "Mitohondrijska" obogatitev je zanimiva, saj obstajajo psevdogeni in paralogi verodostojnih mitohondrijskih proteinov, ki so tarča protiglivičnih kemij. En jasen primer dodatnega pangenoma je paralog sukcinat dehidrogenazne podenote C (SDHC3), za katero je bilo dokazano, da posreduje pri stalni odpornosti proti podrazredu SDHI (zaviralec sukcinat dehidrogenaze) fungicidov pri Z. tritici [45]. Identificirali smo popolne sekvence tega gena le v treh od sedemnajstih sekvenciranih izolatov in odkrili visoko stopnjo genske ekspresije le v enem od 12, ki jih je pozneje proučeval RNAseq (slika 5B). Kljub temu prejšnja študija in naša trenutna analiza poudarjata, da v dodatnem genomu res obstajajo pomembne funkcije, vendar so te verjetno bolj pomembne za prilagajanje spreminjajočim se okoljem kot za osnovni življenjski slog.

Slika 3 Strukturne značilnosti pangenoma in polimorfizmi prisotnosti/odsotnosti v 21 kromosomih referenčnega izolata IPO323. Skupno število kumulativnih mutacij SNP, ki povzročajo modifikatorske, zmerne (M) in visoke (H-izguba funkcije-LoF) spremembe vpliva, izražene kot značilnost povprečne dolžine proteina (aa) na kromosom. B Skupno število kumulativnih mutacij SNP, ki povzročajo zmerne in močne spremembe vpliva, izražene kot značilnost povprečne dolžine proteina na kromosom. C Skupno število kumulativnih mutacij SNP, ki povzročajo spremembe z velikim vplivom, izražene kot značilnost povprečne dolžine proteina na kromosom. D Povprečna povprečna ekspresija vseh genov, prisotnih na vsakem od 21 kromosomov v vseh izolatih. E Polimorfizem prisotnosti in odsotnosti (PaV) genov, predvidenih na jedrnem kromosomu 1 izolata IPO323 v 17 na novo sekvenciranih izolatih. F PaV za gene na jedrnem kromosomu 7. G PaV za gene na akcesornem kromosomu 15. G–F PaV za gene na akcesornem kromosomu 15. Podatki poudarjajo obsežno regionalno variacijo in označujejo jasno razliko med ravnmi polimorfizmov celotnega zaporedja in prisotnostjo/ odsotnost, očitna na jedrnih in pomožnih kromosomih

Slika 4 Predvidena lokalizacija proteinov, kodiranih z jedrnimi in pomožnimi geni. Povzetek odstotnih predvidenih lokalizacij beljakovin, ki jih določi WolfPsort za kategorije, navedene glede na skupne beljakovine, prisotne v jedru in dodatnem pangenomu
Efektorski proteini v dodatnem genomu kažejo večjo variabilnost izražanja med sevi kot tisti v jedru
Več kot osem odstotkov genov v jedrnem genomu je kodiralo domnevne izločene beljakovine, kar je več kot število za dodatni genom (~5 %). Vendar so bili geni v dodatnem genomu, ki kodira izločene beljakovine, pogosteje neznane funkcije, brez prepoznavnih domen ali katalitičnih regij. Ti proteini z neznano funkcijo so znašali približno 75% celotnega dodatnega sekretoma v primerjavi z 42% za jedrni sekretom. Številni kandidati (in v nekaterih primerih potrjeni) efektorji, prisotni v genomu jedra, so bili izraženi v podobnih vzorcih in na primerljivih ravneh v vseh dvanajstih izolatih, ki jih je analiziral RNASeq. Na primer, trije efektorji, ki vsebujejo domeno LysM (Lysin), 3LysM, 1LysM in xLysM, so bili pri vsakem sevu izraženi na zelo podobnih ravneh in v enakih vzorcih (sl. 5C–E). Efektor 3LysM ostaja edina glavna izločena determinanta virulence Z. tritici, kjer ta protein služi za zatiranje rastlinske imunosti, ki jo sproži hitin, med zgodnjo okužbo [46, 47]. Vendar je znano, da vsi trije efektorji LysM delujejo skupaj v ta namen [48]. Zato je treba omeniti, da je bilo med izolati zelo malo variacij v izražanju teh genov, kar potrjuje domneve, da je to obrambno zatiranje ključna sestavina okužbe. Nasprotno pa so kandidatni efektorji, najdeni v dodatnem genomu, pokazali variacijo prisotnosti in odsotnosti ter zelo spremenljivo izražanje med izolati (sl. 5F–H). Na primer, AvrStb6, prvi efektor avirulence, identificiran pri Z. tritici, [49, 50] kaže precejšnje variacije izražanja (slika 5F), kljub temu, da je prisoten v vseh izolatih. To spremenljivko zaporedja, majhen, izločen protein, prepoznajo kultivarji pšenice, ki vsebujejo funkcionalne alele receptorju podobne kinaze Stb6 [25, 51]. To prepoznavanje zagotavlja odpornost proti boleznim proti vsem izolatom, ki vsebujejo določen alel tega efektorja. Med izolati je prišlo do znatne razlike v izražanju AvrStb6 in identificirali smo en izolat (Zt118), pri katerem nismo uspeli odkriti nobenega izražanja v nobenem od treh testiranih pogojev. Iz tega razloga je bil v našem načrtu napovedi AvrStb6 razvrščen v dodatni genom. Mnogi drugi kandidati za efektorje trenutno neznanih funkcij so pokazali pomembno prisotnost/odsotnost in/ali variacijo izražanja v dodatnem genomu (sl. 5G in H).

Slika 5 Sprememba ekspresije genov v jedru in dodatnem pangenomu ter vzpostavitev prehodnega sistema prekomerne ekspresije virusa, uporabljenega za zaslone nekrotrofnih efektorjev. Ključ za interpretacijo podatkov je prikazan na slikah. B Prisotnost/odsotnost in variacija izražanja genov za paralog podenote C sukcinat dehidrogenaze, ki je prisoten v dodatnem genomu. C–E Ekspresijski profili efektorjev ZtLysM, 3LysM, 1LysM in xLysM, ki so vsi prisotni v jedrnem pangenomu. F Ekspresijski profil avirulentnega efektorja AvrStb6. Pomanjkanje kakršnega koli izražanja v izolatu 118 uvršča efektor v akcesorni pangenom. G in H predstavljata primera dodatnih kandidatnih efektorjev v dodatnem pangenomu.
Funkcionalni zasloni ne zagotavljajo nobenega dokaza o nekrotrofni efektorski aktivnosti niti v jedru niti v dodatnem pangenomu
Sprejeli smo nedavno razvit z virusnim vektorjem posredovan prehodni proteinski ekspresijski sistem za pšenico (ter druge žitne in nežitne pridelke) z uporabo virusa Foxtail Mosaic (FoMV) za izvedbo srednje do visoko zmogljivega presejanja kandidatov za Z. tritici efectors iz pangenoma. Posebej smo želeli preveriti, ali ima katera sposobnost induciranja nekroze na majhni plošči kultivarjev pšenice, kar bi lahko pomenilo njihovo funkcijo pri prehodu na simptome bolezni kot "nekrotrofni efektorji" [36, 52]. Za to študijo smo naredili nekaj sprememb v predhodno objavljenem sistemu [53]. Za spodbujanje zunajceličnega izločanja beljakovin v pšenici smo uporabili signalno peptidno zaporedje proteina 1 (TaPR1), povezano s patogenezo pšenice, kodonsko optimizirano za Arabidopsis thaliana, ki je bilo nato zlito v okvirju z vsakim kandidatnim glivičnim efektorskim zaporedjem s sintezo genov (sl. 5I). Učinkovitost signalnega peptida TaPR1 za izločanje funkcionalnih zunajceličnih proteinov Z. tritici je bila ugotovljena z njegovo zmožnostjo induciranja nekroze listov v tobaku, ko je postavljen pred nekrozo Z. tritici in etilen inducirajočemu proteinu (ZtNLP), ki je funkcionalen le ko je usmerjen na zunajcelično izločanje (slika 5 Jl) [54]. Nato smo potrdili, da lahko vektor prekomerno izraža beljakovine enako dobro v različnih kultivarjih pšenice z vizualizacijo lokalnega in sistemskega izražanja zelenega fluorescenčnega proteina (GFP) v listih različnih kultivarjev pšenice (dodatna datoteka 2: slika S3). Končno smo nato preizkusili sposobnost dobro označenega nekrotrofnega efektorja SnToxA iz sorodnega patogena pšenice Parastagonospora nodorum, da inducira nekrozo v listih pšenice genotipov, ki imajo gen za občutljivost Tsn1 [55]. Kot je bilo pričakovano, je čezmerna ekspresija SnToxA, posredovana s FoMV, s signalnim peptidom TaPR1 povzročila nekrozo samo na kultivarju pšenice, ki ima Tsn1 (cv Halberd na sliki 5K), brez simptomov, opaženih na kultivarjih brez tega gena za občutljivost (cv Riband na sliki 5K). ). Ti podatki so potrdili, da je sistem prekomerne ekspresije, ki ga posreduje virusni vektor, primeren za pregledovanje kandidatov za efektorje Z. tritici v večjem obsegu, da se identificirajo vsi z nekrotrofno efektorsko aktivnostjo. Skupno je bilo izbranih 88 kandidatov, ki so bili pregledani proti petim sortam pšenice (dodatna datoteka 5: tabela S3). Ti so obsegali 66 proteinov, ki prebivajo v jedru pangenoma, in 22 iz dodatka. Izbrani geni (dodatna datoteka 5: tabela S3) so segali od jedrnih genov brez polimorfizmov, specifičnih za sev (monomorfnih) in z visoko ekspresijo planta, do tistih v dodatnem genomu, ki kažejo prisotnost/odsotnost in/ali znaten ekspresijski polimorfizem. V vseh poskusih so bile izvedene vzporedne tehnične kontrole ToxA proti cv Halberd in cv Riband, ki so vedno dale pričakovane rezultate. Nasprotno pa nobeden od 88 testiranih prekomerno izraženih proteinov Z. tritici ni povzročil nobene nekroze listov na nobeni sorti pšenice. Če povzamemo, ti rezultati niso zagotovili nobenih dokazov za nekrotrofne efektorje in zato niso podprli nobenega od testiranih kandidatov pri spodbujanju prehoda na nekrotrofno rast med okužbo.

cistanche tubulosa - izboljšanje imunskega sistema
Glavni geni, ki kodirajo proteine z dokazanimi ali predvidenimi funkcijami, ki so bistvene za življenje ali ključne virulence, imajo nižje splošne ravni polimorfizma aminokislin
Izvedli smo iskanje po literaturi, da bi identificirali vse gene Z. tritici, ki so bili predmet funkcionalne karakterizacije, bodisi glede virulence bodisi kot bistveni geni do leta 2018. To je ustvarilo seznam 28 proteinskih zaporedij (dodatna datoteka 6: tabela S4). Podobno smo identificirali seznam 26 proteinov, ki so bili tudi funkcionalno karakterizirani, vendar se je izkazalo, da nimajo pomembne vloge pri virulenci ali da so bistveni (dodatna datoteka 6: tabela S4). Nato smo raziskali ravni kumulativnih redundantnih visokih in zmernih mutacij v teh genih in njihove vrednosti izrazili kot značilnost vsake dolžine proteina ter nato določili povprečne vrednosti za niz. Slika 6 poudarja, da so imeli objavljeni geni, ki vplivajo na virulenco, statistično pomembno nižjo frekvenco (p=0.007) mutacij (polimorfizma) kot tisti, za katere se je izkazalo, da so funkcionalno redundantni.
Študij, namenjenih opredelitvi bistvenih za življenje (esencialnih) genov v filamentoznih glivah (razen kvasovk), je malo in do danes obstaja samo en predstavnik v podatkovni zbirki esencialnih genov (DEG), ki izvira iz oportunističnega človeškega patogena Aspergillus fumigatus [56–58]. Identificirali smo ortologa Z. tritici vseh 28 genov, za katere je eksperimentalno dokazano, da so bistveni za življenje pri A. fumigatus, in znova izračunali relativne stopnje mutacije vsakega glede na dolžine zaporedja (dodatna datoteka 7, tabela S5). Ponovno smo ugotovili jasno statistično značilno zmanjšanje (p=0.0148) v pogostosti visokih in zmernih mutacij SNP v teh kandidatnih bistvenih genih, ki smo jih nato opazili pri genih, za katere se je izkazalo, da niso bistveni ne za virulentnost ne za življenje ( Slika 6). Nasprotno pa ni bilo bistvene razlike (p=0.2128) med stopnjami mutacij za eksperimentalno potrjene virulentne gene in predvidenimi bistvenimi geni (slika 6). Ti podatki skupaj podpirajo koncept, da bi lahko ravni polimorfizmov aminokislin v populacijah uporabili za napovedovanje relativne pomembnosti genov za osnovni življenjski slog organizma.

Slika 6 Analiza osnovnih genskih sklopov eksperimentalno potrjene patogenosti in/ali predvidenih genov, ki so bistveni za življenje, razkriva nižje stopnje mutacije kot pri nebistvenih genih. Povprečne visoke in zmerne (H/M) stopnje mutacije, izražene kot značilnost dolžin proteinov (aa) za sezname genov, ki kodirajo proteine, ki so bili; 1- eksperimentalno ugotovljeno, da nima (ali ima zelo majhno) vlogo pri virulenci gliv; 2-eksperimentalno ugotovljeno, da ima pomembno vlogo pri virulenci in; 3-za katere je bilo predvideno, da kodirajo domnevne gene, ki so bistveni za življenje, prek ortologije v beljakovine, ki so eksperimentalno označene v Aspergillus fumigatus. Simbol zvezdice (*) označuje statistično pomembno razliko med stopnjami mutacije med navedenimi genskimi nizi. Seznami genov in povezani podatki o polimorfizmu so prikazani v dodatni datoteki 6: tabela S4
Uporabnost kombiniranega napovednega pristopa za odkrivanje šibkosti patogena je podprta s študijami genetske komplementacije na petih "jedrnih" mutantih genov za brisanje
Z. tritici je primeren za posredovanje genetskih zaslonov, ki temeljijo na naključni integraciji T-DNA prek glivične transformacije, ki jo posreduje Agrobacterium (AMT). Naše prejšnje delo je ustvarilo zlasti en mutant T-DNA Z. tritici, ki ni mogel povzročiti popolne bolezni na okuženih listih pšenice (slika 7A). Ta mutant, imenovan 23-21 (23. krog preobrazbe in 21. izbrana kolonija), je lahko normalno rasel kot divji tip na hranilno bogatem agarskem mediju (YPD), vendar ni uspel povečati primerljive ravni glivičnih hif, ko je bil gojen na gojišče brez hranil, vključno z vodnim agarjem (slika 7A). Uporabili smo ponovno sekvenciranje 23-21 na osnovi celotnega genoma, da bi razkrili položaj potencialno vzročne vstavke T-DNA. Ta analiza je pokazala eno samo integracijo T-DNA med pozicijama 899878 in 912699 na kromosomu 8, kar je povzročilo izbris/motnjo petih predvidenih kodirnih sekvenc (slika 7B). Analiza SNP in indel ni pokazala nobenih dodatnih neoznačenih mutacij v sevu 23-21 glede na zaporedje genoma divjega tipa IPO323. Delecija 23-21 T-DNA je učinkovito odstranila pet genov, ki so vsi v jedru genoma, in z naslednjimi funkcionalnimi (Interpro) napovedmi; gen 1=citokrom P450; gen 2=S-adenozil metionin metiltransferaza; gen 3=Cink (2) DNA vezavni protein tipa C6; gen 4=nukleozid difosfat kinaze (NDK) in gen 5=glikozil hidrolaze 31 (slika 7B). Raziskali smo relativno število visokih in zmernih mutacij v vsakem proteinu kot značilnost dolžine proteina, kar je pokazalo, da ima protein 4 (NDK) veliko manj mutacij, ki vplivajo na spremembe aminokislinskega zaporedja, kot druge štiri analizirane sekvence v izoliranem nizu (sl. 7C in dodatna datoteka 2: slika S4). Nato smo raziskali povprečno relativno izraženost vseh petih genov pri vseh testiranih izolatih. Razkrilo je tudi, da je bil gen 4 (ki kodira NDK) bistveno bolj izražen kot vsi drugi kandidati (slika 7D in dodatna datoteka 2: slika S5). Tako smo domnevali, da je izguba najmanj polimorfnega in najvišje izraženega gena, gena 4, NDK, odgovorna za izgubo virulence in s tem povezano napako pri podaljšanju hifalnih flamentov. Da bi to preizkusili, smo vsakega od petih kandidatnih genov posamezno transformirali nazaj v mutantni sev 23-21 Z. tritici, pri čemer je vsakega poganjal lasten endogeni promotor. Iz vsakega smo pridobili več transformantov in jih ponovno testirali glede virulence na listih pšenice in sposobnosti podaljšanja nitastih hif na vodnem agarju. To je pokazalo, da je ponovna uvedba samega gena NDK (gen 4) v celoti obnovila tako virulenco kot rast hif na ravni divjega tipa (slika 7E in dodatna datoteka 2: slika S6). Ponovna uvedba vsakega od ostalih štirih kandidatov ni povzročila nobene spremembe fenotipa glede na prvotni mutantni sev 23-21 (slika 7E). Da bi zagotovili, da so bili vsi ponovno uvedeni geni izraženi v svojem ustreznem komplementiranem sevu, je bila izvedena RT-PCR na vsakem od transformantov in prvotnem 23-21 mutantu. To je potrdilo pričakovano pomanjkanje vsakega transkripta v mutantu 23-21 in pokazalo pravilno izražanje vsakega ciljnega gena v dopolnjenih izolatih (slika 7F). Tus, ponovna uvedba enega samega gena z najmanj polimorfizmi na populacijski ravni od petih kandidatov in najvišjo relativno ekspresijo, je obnovila okvarjene fenotipe v tem patogenu pšenice. To eksperimentalno opazovanje podpira uporabnost kombiniranja pangenomike in transkriptomike za napovedovanje genov, ki so potencialno pomembni za ključne funkcionalne življenjske lastnosti.

Slika 7 Testi funkcionalne komplementacije na nepatogenem mutantu Z. tritici z brisanjem petih genov podpirajo kombinirano uporabo stopnje mutacije, pridobljene iz pangenoma, in analize ravni izražanja kot napovedovalca za pomembne ključne gene življenjskega sloga. Značilnosti rasti in okužbe mutanta Z. tritici z naključno vstavitvijo T-DNA "23-21". Sev normalno raste na agarju, bogatem s hranili, vendar ima napako v filamentni rasti na agarju s slabimi hranili in je močno ogrožen pri aktivnosti, ki povzroča bolezni pšeničnih listov. Lestvice predstavljajo 1 cm. B Ponovno sekvenciranje celotnega genoma seva 23-21 razkrije T-DNA posredovano izbris 13 kb genomske regije, ki moti ali izbriše pet predvidenih genov iz osrednjega pangenoma. C Prikazuje povprečne dogodke visoke in zmerne mutacije za vsak gen (označen z 1-5) iz pangenoma glede na dolžino kodiranega proteina (aa)
Diskusija
Kombinirano pangenomiko in transkriptomiko je mogoče uporabiti kot orožje proti hitro razvijajočim se patogenom
Pangenomics analyses have been performed on other fungi and yeasts including Saccharomyces cerevisiae, Candida albicans, Cryptococcus neoformans var. grubii, and Aspergillus fumigatus [10]. All four species are model organisms in eukaryotic genomics and the latter three can also cause human diseases. Recent pangenome analyses on each of these species revealed that > 80% of all genes detected were core and thus found in every strain [10]. Our current study, and those previously [27, 28], clearly highlight that Z. tritici has a larger (>40 % vseh genov) dodatnega genoma kot te vrste. Zakaj in kako Z. tritici in potencialno druge rastlinsko patogene glive ohranjajo tako veliko dodatno komponento, ni jasno. Najmanjših osem kromosomov, opredeljenih v IPO323, na primer nima jasnega večjega vpliva na virulenco ali druge procese, pri čemer samo ena študija trenutno kaže, da imajo kromosomi 14, 16, 18, 19 in 21 subtilno vlogo pri virulentnosti na izbrane sorte pšenice [59]. Kljub temu se kombinacije teh majhnih kromosomov ohranjajo v populacijah. Predlagano je bilo, da zagotavljajo dogodke rekombinacije, ki so lahko osnova za sposobnost glive, da se hitro razvije, da se prilagodi okoljskim obremenitvam, potencialno v kombinaciji z visokimi stopnjami aktivnosti prenosljivih elementov [60–62]. Podoben primer lahko trdimo za velik dodatni genom. Podporo za to zagotavlja funkcionalni pomen dveh pomožnih komponent genoma, omenjenih v tej študiji, paraloga podenote C SDH in AvrStb6, ki imata obe ključni vlogi pri interakciji s spremenljivimi elementi zunanjega okolja (nanašanje fungicidov in kultivarji z ujemanjem geni za odpornost na bolezni) [25, 45]. Opisani so bili tudi drugi biološki procesi, ki se lahko tudi izgubijo v posameznih izolatih Z. tritici brez očitnih okvar primernosti, vključno z nadzorom melanizacije (pigmentacije) [63]. Naša študija je poudarila, da bi lahko pomožni, hitro razvijajoči se genom Z. tritici potencialno uporabili proti njej, če se namesto tega osredotočimo na tisto, kar ni mogoče izgubiti ali ima omejen polimorfizem. Ta študija je to skušala doseči z upoštevanjem jedrnih genov, ki niso samo prisotni in funkcionalni v vseh izolatih, ampak so vsi izolati tudi izraženi. Uporabili smo tudi pristop poskusa razvrščanja genskih sklopov v jedrnem genomu na podlagi ravni variabilnosti aminokislinskega zaporedja. Seveda obstaja nekaj opozoril pri metodah, ki smo jih uporabili, zlasti v tem, da redundantnih (enakega tipa in položaja) mutacij ni mogoče zlahka ločiti od podobnega števila mutacij, ki se lahko pojavijo na edinstvenih mestih v vsakem izolatu (neredundantne mutacije). Tako naša metoda ni primerna za razvrščanje hitro razvijajočih se genov. Kljub temu metoda omogoča enostavno identifikacijo genov brez in nizke variabilnosti na podlagi nizkih stopenj polimorfizmov, ki vplivajo na spremembe aminokislin. Pristop je pokazal, da so eksperimentalno preverjeni in predvideni za življenje bistveni geni ali virulentni geni imeli med izolati bistveno manj polimorfizma te vrste kot tisti, katerih funkcije so nepogrešljive za te procese. Nazadnje smo ta pristop razširili na identifikacijo nove virulentne funkcije nukleozid difosfat kinaze (NDK), ki je pokazala najmanj variacij vseh genov v 5-genski deleciji T-DNA. Na podlagi teh ugotovitev predlagamo, da bi lahko ravni polimorfizma v jedrnih genih, identificiranih v pangenomiki, uporabili za sklepanje o pomembnih funkcijah za kodirane proteine in s tem dajanje prednosti genom za funkcionalno analizo za identifikacijo novih ciljev za zaščito pridelka in potencialno zdravje živali.
Pojavljajoča se slabost v biologiji okužbe z Z. tritici in sorodnimi patogeni?
Ta študija je zagotovila tudi nadaljnje specifične vpoglede v biologijo okužbe tega pomembnega patogena pšenice. Prvič, pridobljeni niso bili nobeni dokazi, ki bi podpirali prisotnost večjih nekrotrofnih efektorskih aktivnosti za 88 izločenih proteinov, izbranih iz jedrnega in pomožnega genoma. Ne moremo zavreči možnosti, da nismo izbrali pravilnih proteinov ali da bi več efektorjev lahko delovalo skupaj, da bi sprožilo smrt rastlinske celice (kar nakazujejo tudi podobni profili izražanja). Če je tako slednje, bi se to razlikovalo od jasnega pomena posameznih nekrotrofnih efektorjev v sorodnih glivah, ki okužijo pšenico, zlasti vrstah Parastagonospora nodorum in Pyrenophora [35]. Možno je tudi, da so ravni izražanja, ki jih izpeljemo iz prehodnega sistema FoMV, nižje od tistih, ki so potrebne za efektorje, katerih prepoznavanje je manj izrazito kot pri SnToxA. Kljub temu tukaj predstavljeni podatki ne podpirajo ideje, da sta prehod na simptomatsko rast in smrt rastlinske celice sprožena s prepoznavanjem glavnih (enotnih) nekrotrofnih efektorjev Z. tritici. Zato je možno, da množična proizvodnja teh proteinov ob pojavu simptomov namesto tega služi za zaščito glivičnih hif pred očitno hiperaktivacijo celične smrti in odzivom rastlin. V skladu s tem se je izkazalo, da imajo izločeni efektorji iz te in drugih gliv sposobnost zaviranja rastlinskih proteaz, hitinaz in drugih encimov, ki napadajo celično steno, ki jih same inducirajo rastline med obrambnimi odzivi [46, 48, 64, 65]. ]. Pred kratkim se je tudi pokazalo, da glivični efektorji manipulirajo in preoblikujejo mikro in mikrobiome [66, 67].

koristi cistanche za moške - krepitev imunskega sistema
Vendar pa je pomembna ugotovitev ključne vloge pri virulenci za NDK. Tem proteinom so pripisali številne funkcije različnih prokariontskih in evkariontskih organizmov. Pri glivah obstaja eno poročilo, ki pripisuje vlogo modulaciji rastlinske imunosti [68], medtem ko je bila pri drugi vrsti (A. fumigatus) dokazana funkcija, ki je bistvena za življenje [69]. Vendar je primarna in ohranjena funkcija teh proteinov fosforilacija nukleozid difosfatov, običajno z uporabo ATP kot substrata, za ustvarjanje drugih nukleozid trifosfatov (NTP), potrebnih za pomoč pri spodbujanju različnih celičnih procesov [70, 71]. To je še posebej pomembno, kadar omejeni viri otežijo ustvarjanje določenih NTP z drugimi sredstvi. Tako pa NDK predstavljajo ključno dejavnost reševalne poti za regeneracijo NTP, ki je najverjetneje pomembna, ko so zunajcelični viri omejeni. Pomembne vloge za številne druge reševalne poti, zlasti biosintetske poti, so pred kratkim izšle iz drugih študij delovanja genov na Z. tritici. Na primer, biosinteza lizina je bistvena za okužbo in rast hif na slabih hranilih [72], kot je biosinteza purina [73]. Te funkcije so redundantne za rast na celotnem mediju. Prejšnji podatki o transkriptomih o zelo zgodnji fazi kolonizacije površine listov so pokazali, da je gliva v okolju, ki je osiromašeno s hranili in je odvisna od uporabe znotrajceličnih zalog [33]. Skupaj s prejšnjimi funkcionalnimi študijami in ključno vlogo, prikazano za NDK, je jasno, da je Z. tritici izjemno ranljiva za inhibicijo ključnih biosintetskih in rešilnih poti, ko je na površini listov med zgodnjo kolonizacijo, in potencialno do indukcije smrt rastlinske celice približno 7-10 dni kasneje. Tako bi lahko nova sredstva za zaščito pridelka ali strategije usmerili v zaviranje teh procesov, ki lahko predstavljajo slabost pri Z. tritici in potencialno za veliko različnih drugih sorodnih gliv s podobnimi načini okužbe.
Sklepi
Ta študija zagotavlja začetno podporo za kombinirano uporabo pangenomike in transkriptomike za definiranje genov, ki predstavljajo jedro in potencialno izkoriščene slabosti pri hitro razvijajočih se patogenih. Vendar bi načeloma lahko pristope uporabili za določanje prednosti genov v katerem koli biološkem sistemu, kjer je na voljo več genomov in transkriptomov. Predvidevamo, da bi lahko ti pristopi pospešili odkrivanje temeljnih bioloških procesov v številnih različnih bioloških sistemih.
Reference
1. Fisher MC, Hawkins NJ, Sanglard D, Gurr SJ. Pojav odpornosti na protiglivična zdravila po vsem svetu predstavlja izziv za zdravje ljudi in prehransko varnost. Znanost. 2018;360. https://doi.org/10.1126/science.aap7999.
2. Fisher MC, Henk DA, Briggs CJ, Brownstein JS, Madoff LC, McCraw SL, et al. Nastajajoče glivične grožnje zdravju živali, rastlin in ekosistemov. Narava. 2012;484. https://doi.org/10.1038/nature10947.
3. Lucas JA, Hawkins NJ, Fraaije BA. Razvoj odpornosti na fungicide. Adv Appl Microbiol. 2015;90. https://doi.org/10.1016/bs.aambs.2014.09.001.
4. Heitman J. Spolno razmnoževanje in razvoj mikrobnih patogenov. Curr Biol. 2006;16. https://doi.org/10.1016/j.cub.2006.07.064.
5. Dong S, Raffaele S, Kamoun S. Genomi dveh hitrosti filamentnih patogenov: valček z rastlinami. Curr Opin Genet Dev. 2015; 35: 57–65. https://doi.org/10.1016/J.GDE.2015.09.001.
6. Tettelin H, Masignani V, Cieslewicz MJ, Donati C, Medini D, Ward NL, et al. Analiza genoma več patogenih izolatov Streptococcus aga‑lactiae: posledice za mikrobni "pan-genom". Proc Natl Acad Sci US A. 2005;102. https://doi.org/10.1073/pnas.0506758102.
7. Lefébure T, Stanhope MJ. Evolucija jedra in pangenoma streptokoka do koka: pozitivna selekcija, rekombinacija in sestava genoma. Genome Biol. 2007;8. https://doi.org/10.1186/gb-2007-8-5-r71.
8. Tian CF, Zhou YJ, Zhang YM, Li QQ, Zhang YZ, Li DF, et al. Primerjalna genomika soje, ki nodulira rhizobia, kaže na obsežno pridobivanje genov, specifičnih za rod, v prilagoditvah. Proc Natl Acad Sci US A. 2012;109. https://doi.org/10.1073/pnas.1120436109.
9. Syme RA, Tan KC, Rybak K, Friesen TL, McDonald BA, Oliver RP, et al. Primerjalna analiza genoma Panparastagonospora - napoved efektorja in evolucija genoma. Genome Biol Evol. 2018;10. https://doi.org/10.1093/gbe/evy192.
10. McCarthy CGP, Fitzpatrick DA. Pangenomske analize modelnih vrst gliv. Microb. Genomika. 2019;5. https://doi.org/10.1099/mgen.0.000243.
11. Yang X, Li Y, Zang J, Li Y, Bie P, Lu Y, et al. Analiza pan-genoma za identifikacijo jedrnih genov in bistvenih genov Brucella spp. Mol Gen Genomics. 2016;291. https://doi.org/10.1007/s00438-015-1154-z.
12. Barber AE, Sae-Ong T, Kang K, Seelbinder B, Li J, Walther G, et al. Vsegenomska analiza Aspergillus‑lus fumigatus identificira genetske različice, povezane z okužbo pri ljudeh. Nat Microbiol. 2021;6. https://doi.org/10.1038/ s41564-021-00993-x.
13. Zhang X, Liu B, Zou F, Shen D, Yin Z, Wang R, et al. Ponovno sekvenciranje celotnega genoma razkriva naravno variacijo in prilagodljiv razvoj Phytophthora sojae. Front Microbiol. 2019;10. https://doi.org/10.3389/fmicb.2019. 02792.
14. Torriani SFF, Melichar JPE, Mills C, Pain N, Sierotzki H, Courbot M. Zymoseptoria tritici: velika grožnja pridelavi pšenice, integrirani pristopi k nadzoru. Gljivične Genet Biol. 2015;79. https://doi.org/10. 1016/j.fgb.2015.04.010.
15. Zhan J, Mundt CC, McDonald BA. Merjenje priseljevanja in spolnega razmnoževanja v poljskih populacijah Mycosphaerella graminicola. Fitopatologija. 1998;88. https://doi.org/10.1094/PHYTO.1998.88.12.1330.
16. Zhan J, Kema GHJ, Waalwijk C, McDonald BA. Porazdelitev alelov tipa parjenja pri patogenu pšenice Mycosphaerella graminicola po prostorskih lestvicah od lezij do celin. Gljivične Genet Biol. 2002;36. https://doi. org/10.1016/S1087-1845(02)00013-0.
17. Stukenbrock EH, Banke S, Javan-Nikkhah M, McDonald BA. Izvor in udomačitev glivičnega patogena pšenice Mycosphaerella gramini‑cola prek simpatrične speciacije. Mol Biol Evol. 2007;24. https://doi.org/10. 1016/S1087-1845(02)00013-0.
18. Linde CC, Zhan J, McDonald BA. Struktura populacije Mycosphaer‑lla graminicola: od lezij do celin. Fitopatologija. 2002;92. https://doi.org/10.1094/PHYTO.2002.92.9.946.
19. Croll D, McDonald BA. Genetska osnova lokalne prilagoditve za patogene glive v kmetijskih ekosistemih. Mol Ecol. 2017;26. https://doi.org/ 10.1111/mec.13870.
20. Croll D, Lendenmann MH, Stewart E, McDonald BA. Vpliv rekombinacijskih vročih točk na razvoj genoma glivičnega rastlinskega patogena. Genetika. 2015;201. https://doi.org/10.1534/genetics.115.180968.
21. Dutta A, Croll D, McDonald BA, Barrett LG. Vzdrževanje variabilnosti virulence in razmnoževanja v populacijah patogena kmetijskih rastlin. Evol Appl. 2021;14. https://doi.org/10.1111/eva.13117.
22. Feurtey A, Stevens DM, Stephan W, Stukenbrock EH, Stajich J. Interspecifična genska izmenjava uvaja visoko genetsko variabilnost pri patogenih pridelkih. Genome Biol Evol. 2019;11. https://doi.org/10.1093/gbe/evz224.
23. Hartmann FE, Sánchez-Vallet A, McDonald BA, Croll D. Gljivični patogen pšenice je razvil specializacijo gostitelja z obsežnimi kromosomskimi preureditvami. ISME J. 2017; 11. https://doi.org/10.1038/ismej.2016.196.
24. Fouché S, Plissonneau C, McDonald BA, Croll D. Mejoza vodi do vsesplošne variacije števila kopij in popačenega dedovanja akcesornih kromo‑ mov patogena pšenice Zymoseptoria tritici. Genome Biol Evol. 2018;10. https://doi.org/10.1093/gbe/evy100.
25. Stephens C, Ölmez F, Blyth H, McDonald M, Bansal A, Burcu Turgay E, et al. Izjemne nedavne spremembe v genetski raznolikosti gena za avirulence AvrStb6 v svetovnih populacijah patogena pšenice Zymoseptoria tritici. Mol Plant Pathol. 2021. https://doi.org/10.1111/mpp.13101.
26. Goodwin SB, M'Barek S, Dhillon B, Wittenberg AHJ, Crane CF, Hane JK, et al. Končni genom glivičnega patogena pšenice Mycosphaerella graminicola razkriva razpršeno strukturo, plastičnost kromosomov in prikrito patogenezo. PLoS Genet. 2011;7. https://doi.org/10.1371/journal.pgen.1002070.
27. Badet T, Oggenfuss U, Abraham L, McDonald BA, Croll D. 19-izolat globalnega pangenoma referenčne kakovosti za glivičnega patogena pšenice Zymoseptoria tritici. BMC Biol. 2020;18. https://doi.org/10.1186/ s12915-020-0744-3.
28. Plissonneau C, Hartmann FE, Croll D. Pangenomske analize patogena pšenice Zymoseptoria tritici razkrivajo strukturno osnovo zelo plastičnega evkariontskega genoma. BMC Biol. 2018;16. https://doi.org/10.1186/ s12915-017-0457-4.
29. Wittenberg AHJ, van der Lee TAJ, M'Barek SB, Ware SB, Goodwin SB, Kilian A, et al. Mejoza poganja izjemno plastičnost genoma pri haploidnem glivičnem rastlinskem patogenu Mycosphaerella graminicola. PLoS One. 2009;4. https://doi.org/10.1371/journal.pone.0005863.
30. Steinberg G. Celična biologija Zymoseptoria tritici: organizacija patogenih celic in okužba pšenice. Gljivične Genet Biol. 2015;79. https://doi.org/10. 1016/j.fgb.2015.04.002.
31. Kema GHJ, Yu DZ, Rijkenberg FHJ, Shaw MW, Baayen RP. Histologija patogeneze Mycosphaerella graminicola v pšenici. Fitopatologija. 1996;86. https://doi.org/10.1094/Phyto-86-777.
32. Rudd JJ, Kanyuka K, Hassani-Pak K, Derbyshire M, Andongabo A, Devon-Shire J, et al. Profiliranje transkriptoma in metabolita cikla okužbe z Zymoseptoria tritici na pšenici razkriva dvofazno interakcijo z rastlinsko imunostjo, ki vključuje diferencialne kromosomske prispevke patogenov in variacijo definicije hemibiotrofnega načina življenja. Plant Physiol. 2015;167. https://doi.org/10.1104/pp.114.255927.
33. Keon J, Antoniw J, Carzaniga R, Deller S, Ward JL, Baker JM, et al. Transkripcijska prilagoditev Mycosphaerella graminicola na programirano celično smrt (PCD) njenega občutljivega pšeničnega gostitelja. Mol interakcija med rastlinami in mikrobi. 2007;20. https://doi.org/10.1094/MPMI-20-2-0178.
34. Rudd JJ, Keon J, Hammond-Kosack KE. Pšenični mitogen-aktivirani proteinski kinazi TaMPK3 in TaMPK6 sta različno regulirani na več ravneh med združljivimi interakcijami bolezni z Mycosphaerella graminicola. Plant Physiol. 2008;147. https://doi.org/10.1104/pp.108. 119511.
35. Friesen TL, Faris JD. Karakterizacija interakcij efektor-tarča v nekrotrofnih patosistemih razkriva trende in variacije v manipulaciji gostitelja. Annu Rev Phytopathol. 2021;59. https://doi.org/10.1146/annur ev-phyto-120320-012807.
36. Friesen TL, Faris JD, Solomon PS, Oliver RP. Gostiteljski specifični toksini: povzročitelji nekrotrofne patogenosti. Cell Microbiol. 2008;10. https://doi.org/10. 1111/j.1462-5822.2008.01153.x.
37. Ben M'Barek S, Cordewener JHG, Tabib Ghafary SM, van der Lee TAJ, Liu Z, Mirzadi Gohari A, et al. FPLC in masna spektrometrija s tekočinsko kromatografijo identificirata kandidatne proteine, ki povzročajo nekrozo, iz filtratov kulture glivičnega patogena pšenice Zymoseptoria tritici. Gljivične Genet Biol. 2015;79. https://doi.org/10.1016/j.fgb.2015.03.015.
38. Wyka S, Mondo S, Liu M, Nalam V, Broders K. Velik dodatni genom in visoke stopnje rekombinacije lahko vplivajo na globalno porazdelitev in širok razpon gostiteljev glivičnega rastlinskega patogena Claviceps purpurea. PLoS One. 2022;17. https://doi.org/10.1371/journal.pone.0263496.
39. Moolhuijzen PM, Glej PT, Shi G, Powell HR, Cockram J, Jørgensen LN, et al. Globalni pangenom za pšenični glivični patogen Pyrenophora triticirepentis in napoved strukturne homologije efektorskega proteina. Microb. Genomika. 2022;8. https://doi.org/10.1371/journal.pone.0263496.
40. Kema GHJ, Sayoud R, Annone JG, Van Silfhout CH. Genetske variacije za virulentnost in odpornost v sistemu poti pšenice in Mycosphaerella graminicola II. Analiza interakcij med izolati patogenov in gostiteljskimi sortami. Fitopatologija. 1996;86. https://doi.org/10.1094/Phyto-86-213.
41. Kema GHJ, Annone JG, Sayoud R, Van Silfhout CH, Van Ginkel M, De Bree J. Genetske variacije za virulentnost in odpornost v patosistemu pšenice Mycosphaerella graminicola I. interakcije med izolati patogenov in gostiteljskimi kultivarji. Fitopatologija. 1996;86. https://doi.org/ 10.1094/Phyto-86-200.
42. Zhan J, Pettway RE, McDonald BA. Za globalno genetsko strukturo patogena pšenice Mycosphaerella graminicola je značilna velika jedrska raznolikost, nizka mitohondrijska raznolikost, redna rekombinacija in pretok genov. Gljivične Genet Biol. 2003;38. https://doi.org/10.1016/S1087- 1845(02)00538-8.
43. Palma-Guerrero J, Torriani SFF, Zala M, Carter D, Courbot M, Rudd JJ, et al. Primerjalne transkriptomske analize sevov Zymoseptoria tritici kažejo zapletene prehode v življenjskem slogu in intraspecifično variabilnost transkripcijskih profilov. Mol. Rastlina Pathol. 2016;17. https://doi.org/10.1111/mpp.12333.
44. Kellner R, Bhattacharyya A, Poppe S, Hsu TY, Brem RB, Stukenbrock EH. Ekspresijsko profiliranje patogena pšenice Zymoseptoria tritici razkriva genomske vzorce transkripcije in regulatorne programe, specifične za gostitelja. Genome Biol Evol. 2014;6. https://doi.org/10.1093/gbe/evu101.
45. Steinhauer D, Salat M, Frey R, Mosbach A, Luksch T, Balmer D, et al. Nepogrešljiv paralog podenote C sukcinat dehidrogenaze posreduje stalno odpornost proti podrazredu fungicidov SDHI pri Zymoseptoria tritici. Patog PLoS. 2019;15. https://doi.org/10.1371/journal.ppat. 1007780.
46. Marshall R, Kombrink A, Motteram J, Loza-Reyes E, Lucas J, Hammond Kosack KE, et al. Analiza dveh v rastlinah izraženih homologov efektorja LysM iz glive Mycosphaerella graminicola razkriva nove funkcionalne lastnosti in različne prispevke k virulenci pri pšenici. Plant Physiol. 2011;156. https://doi.org/10.1104/pp.111.176347.
47. Lee WS, Rudd JJ, Hammond-Kosack KE, Kanyuka K. Prikrita patogeneza seznama Mycosphaerella graminicola, ki jo posreduje efektor, spodkopava prepoznavanje prek homologov cerk1 in cebip v pšenici. Mol interakcija med rastlinami in mikrobi. 2014;27. https://doi.org/10.1104/pp.111.176347.
48. Tian H, MacKenzie CI, Rodriguez-Moreno L, van den Berg GCM, Chen H, Rudd JJ, et al. Trije LysM efektorji Zymoseptoria tritici skupaj razorožijo imunost rastlin, ki jo sproži hitin. Mol Plant Pathol. 2021;22. https:// doi.org/10.1104/pp.111.176347.
49. Zhong Z, Marcel TC, Hartmann FE, Ma X, Plissonneau C, Zala M, et al. Majhna izločena beljakovina v Zymoseptoria tritici je odgovorna za avirulenco na kultivarjih pšenice, ki nosijo gen za odpornost Stb6. Novi Phytol. 2017;214. https://doi.org/10.1111/nph.14434.
50. Kema GHJ, Mirzadi Gohari A, Aouini L, Gibriel HAY, Ware SB, Van Den Bosch F, et al. Stres in spolno razmnoževanje vplivata na dinamiko efektorja toplotnega patogena AvrStb6 in odpornost na strobilurin. Nat Genet. 2018;50. https://doi.org/10.1111/nph.14434.
51. Saintenac C, Lee WS, Cambon F, Rudd JJ, King RC, Marande W, et al. Protein Stb6, podoben pšeničnemu receptorju-kinazi, nadzoruje odpornost gena za gen na glivični patogen Zymoseptoria tritici. Nat Genet. 2018;50. https://doi.org/ 10.1038/s41588-018-0051-x.
52. Tan KC, Oliver RP, Solomon PS, Mofat CS. Proteinski nekrotrofni efektorji pri virulenci gliv. Funct Plant Biol. 2010;37. https://doi.org/10. 1071/FP10067.
53. Bouton C, King RC, Chen H, Azhakanandam K, Bieri S, Hammond-Kosack KE, et al. Virus mozaika lisičjega repa: virusni vektor za izražanje beljakovin v žitih. Plant Physiol. 2018;177. https://doi.org/10.1104/pp.17.01679.
54. Motteram J, Küfner I, Deller S, Brunner F, Hammond-Kosack KE, Nürnberger T, et al. Molekularna karakterizacija in funkcionalna analiza MgNLP, edinega proteina, ki vsebuje domeno NPP1, iz glivičnega patogena listov pšenice mycosphaerella graminicola. Mol interakcija med rastlinami in mikrobi. 2009;22. https://doi.org/10.1094/MPMI-22-7-0790.
55. Faris JD, Zhang Z, Lu H, Lu S, Reddy L, Cloutier S, et al. Edinstven gen, podoben odpornosti na bolezni pšenice, uravnava občutljivost, ki jo sproži efektor, za nekrotrofne patogene. Proc Natl Acad Sci US A. 2010;107. https://doi. org/10.1094/MPMI-22-7-0790.
56. Lu Y, Deng J, Rhodes JC, Lu H, Lu LJ. Napovedovanje bistvenih genov za prepoznavanje potencialnih tarč zdravil pri Aspergillus fumigatus. Comput Biol Chem. 2014;50. https://doi.org/10.1016/j.compbiolchem.2014.01.011.
57. Osmani AH, Oakley BR, Osmani SA. Identifikacija in analiza esencialnih genov Aspergillus nidulans z uporabo tehnike reševanja heterokarionov. Nat Protoc. 2006;1. https://doi.org/10.1038/nprot.2006.406.
58. Hu W, Sillaots S, Lemieux S, Davison J, Kaufman S, Breton A, et al. Identifikacija bistvenih genov in prednostna naloga zdravil pri Aspergillus fumigatus. Patog PLoS. 2007;3. https://doi.org/10.1371/journal.ppat. 0030024.
59. Habig M, Quade J, Stukenbrock EH. Napredni genetski pristop razkriva pomen pomožnih kromosomov v glivičnem pšeničnem patogenu Zymoseptoria tritici, ki je odvisen od genotipa gostitelja. MBio. 2017;8. https://doi. org/10.1128/mBio.01919-17.
60. Fouché S, Badet T, Oggenfuss U, Plissonneau C, Francisco CS, Croll D. Dinamika derepresije prenosljivih elementov, ki jih poganja stres, in razvoj virulence pri glivičnem patogenu. Mol Biol Evol. 2020;37. https://doi. org/10.1093/molbev/msz216.
61. Möller M, Habig M, Freitag M, Stukenbrock EH. Izredna nestabilnost genoma in razširjene kromosomske preureditve med vegetativno rastjo. Genetika. 2018;210. https://doi.org/10.1534/genetics.118.301050.
62. Bertazzoni S, Williams AH, Jones DA, Syme RA, Tan KC, Hane JK. Dodatki naredijo opremo: pomožni kromosomi in druge pogrešljive regije DNK v rastlinsko-patogenih glivah. Mol interakcija med rastlinami in mikrobi. 2018;31. https://doi.org/10.1094/mpmi-06-17-0135-f.
63. Krishnan P, Meile L, Plissonneau C, Ma X, Hartmann FE, Croll D, et al. Vstavki prenosljivih elementov oblikujejo regulacijo genov in proizvodnjo melanina v glivičnem patogenu pšenice. BMC Biol. 2018;16. https://doi. org/10.1094/mpmi-06-17-0135-f.
64. Sánchez-Vallet A, Tian H, Rodriguez-Moreno L, Valkenburg DJ, Saleem Batcha R, Wawra S, et al. Izločeni LysM efektor ščiti glivične hife s homodimerno polimerizacijo, odvisno od hitina. Patog PLoS. 2020;16. https://doi.org/10.1371/journal.ppat.1008652.
65. Breen S, Williams SJ, Winterberg B, Kobe B, Solomon PS. Proteini PR-1 pšenice so tarča efektorskih proteinov nekrotrofnih patogenov. Rastlina J. 2016;88. https://doi.org/10.1111/tpj.13228.
66. Snelders NC, Petti GC, van den Berg GCM, Seidl MF, Thomma BPHJ. Starodavni protimikrobni protein, ki ga je vključil glivični rastlinski patogen za manipulacijo mikobioma planta. Proc Natl Acad Sci US A. 2021; 118. https://doi.org/10.1073/pnas.2110968118.
67. Snelders NC, Rovenich H, Petti GC, Rocafort M, van den Berg GCM, Vorholt JA, et al. Manipulacija mikrobioma s patogenom glivičnih rastlin, ki se prenaša v tleh, z uporabo efektorskih proteinov. Nat rastline. 2020. https://doi.org/10. 1038/s41477-020-00799-5.
68. Rocha RO, Wilson RA. Magnaporthe oryzae nukleozid difosfat kinaza je potrebna za presnovno homeostazo in redoks posredovano zatiranje prirojene imunosti gostitelja. Mol Microbiol. 2020;114. https://doi.org/ 10.1111/mmi.14580
