Imunski odziv pri COVID-19: kaj je naslednje?
Sep 12, 2023
Koronavirusna bolezen 2019 (COVID-19) je svetovna pandemija že več kot 2 leti in še vedno vpliva na naš vsakodnevni življenjski slog in kakovost na načine brez primere. Nujno je potrebno boljše razumevanje imunosti in njene regulacije kot odziva na okužbo s SARS-CoV-2. Na podlagi trenutne literature tukaj pregledujemo različne mutacije virusa in razvijajoče se manifestacije bolezni skupaj s spremembami imunskih odzivov s posebnim poudarkom na prirojenem imunskem odzivu, zunajceličnih pasteh nevtrofilcev, humoralni imunosti in celični imunosti. Različne vrste cepiv so primerjali in analizirali na podlagi njihovih edinstvenih lastnosti, da izzovejo specifično imunost. Razpravljali so o različnih terapevtskih strategijah, kot so protitelesa, protivirusna zdravila in nadzor vnetja. Predvidevamo, da bo z razpoložljivimi in nenehno nastajajočimi novimi tehnologijami, zmogljivejšimi cepivi in urniki dajanja, učinkovitejšimi zdravili in boljšimi javnozdravstvenimi ukrepi pandemija COVID-19 kmalu pod nadzorom.

koristi dodatka cistanche - kako okrepiti imunski sistem
DEJSTVA
1. Imunski odzivi, povezani z okužbo SARS-CoV-2, so osrednjega pomena za patogenezo COVID-19.
2. Prirojeni imunski sistemi zaznavajo virusno RNK prek TLR3, TLR7 in RIG-1 in hiperaktivirajo prirojene imunske odzive.
3. Neregulirane tvorbe zunajceličnih pasti nevtrofilcev (NET) inducirajo imunsko trombozo in poslabšajo vnetje v pljučih bolnikov s COVID-19.
4. Limfocitopenija, povzročena z apoptozo in tvorbo sincicija, spodbuja napredovanje COVID-19. 5. Cepiva proti SARS-CoV-2 pogosto niso mogla blokirati okužbe, vendar so zagotovila imunost za zmanjšanje resnosti bolezni.
ODPRTA VPRAŠANJA
1. Kako ugotoviti pomen specifičnih celic CD8+ T pri imunosti na SARS-CoV-2?
2. Kako se bo končala pandemija COVID-19? Bo COVID-19 postal endemičen?
3. Kako se bo razvijala različica Omicron? Kakšne imunske lastnosti bo imela naslednja varianta?
4. Ali bo čredna imunost, zgrajena s cepljenjem in naravnimi okužbami, končala prenos virusa SARS-CoV-2?
Pandemične nalezljive bolezni so večkrat povzročile škodo v človeški družbi, vključno s časi »atenske kuge« (več kot 100 000 smrti leta 430 pr. n. št.), Yersinia pestis (50 milijonov smrti leta 1340) ali »španske gripe«. « (50 milijonov smrti leta 1918). Sem spadajo tudi številne virusne bolezni, kot je HIV (40 milijonov smrti v letih 1980–2000), H1N1 "prašičja gripa" (300.000 smrti v letu 2009), rumena mrzlica, zika, ebola, SARS, MERS in sedanji koronavirus bolezen 2019 (COVID-19), ki jo povzroča hud akutni respiratorni sindrom CoronaVirus 2 (SARS-CoV-2). Kljub temu sta minili že več kot dve leti od prvega pojava COVID-19, ta pandemija pa še vedno vpliva na življenjski slog, gospodarske dejavnosti in družbeno vedenje našega sveta [1]. Z več kot 500 milijoni potrjenih primerov COVID-19 (več kot 6 % svetovnega prebivalstva) in približno 6,5 milijona smrti po vsem svetu kaže povzročiteljski virus SARS-CoV-2 [2–6], ki se hitro širi genealogija zdaj upravičuje razvrstitev za vsaj 13 različic in zdi se, da je postala endemična, z mutacijami na N-koncu in receptorskem vezavnem območju, vključno s p.Glu484Lys, ki ga najdemo v najnevarnejših različicah [7], slika 1. Različice zaskrbljujoči (VoC) so bili Alpha, Beta (B.1.351), Gamma (P.1), Delta (B.1.617.2) in Omicron (B.1.1.529), pri čemer sta Delta in Omicron najbolj zaskrbljujoča tiste [8]. Grozljivo je, da se je pojavila nova različica s hrbtenico Delta in konico Omicron [9]. Velik napredek je bil dosežen pri obvladovanju pandemije COVID-19, vendar se večina prizadevanj še vedno osredotoča na zmanjšanje okužbe in resnosti bolezni s cepljenjem (danih več kot 11 milijard odmerkov cepiva) [10–12], kar je občasno povzročilo nekateri neželeni učinki [13]. Medtem se virus razvija v različice z visoko stopnjo prenosa in nizko patogenostjo [14]. Na žalost je skoraj gotovo, da bo virus dobil nove mutacije, po možnosti z večjo patogenostjo. Tukaj pregledujemo jin in jang prirojene in adaptivne imunosti na akutno okužbo s SARS-CoV-2 in poudarjamo odprta odprta vprašanja.

Slika 1 Mutacijska pokrajina koničastih proteinov izbranih različic SARS-CoV-2. Zgornja plošča prikazuje profil mutacije in razširjenost koničastih proteinov v 13 linijah SARS-CoV-2, ki so prejele grško oznako, in 7 nedavno razvitih različic SARS-CoV-2, ki so pritegnile pozornost javnosti. Starševske linije novih različic SARS-CoV-2 so prikazane v tabeli. Spodnje slike prikazujejo stranski in zgornji pogled na 3-dimenzionalno strukturo za beljakovino konice Omicron s preslikanimi mutacijskimi aminokislinami [170]. Opomba: Insercijske mutacije niso profilirane.
OSNOVNA VNETNA STANJA IN RESNOST OKUŽBE
Večina ljudi, okuženih s SARS-CoV-2, ima blago do zmerno bolezen dihal, vključno z zvišano telesno temperaturo, kašljem, zasoplostjo, bolečinami v mišicah, glavobolom, izgubo okusa in vonja, vnetim grlom, zamašenostjo ali izcedkom iz nosu; medtem ko nekateri resno zbolijo in potrebujejo zdravniško pomoč, zlasti starejši in tisti z osnovnimi zdravstvenimi težavami, kot so bolezni srca in ožilja, sladkorna bolezen, kronične bolezni dihal ali rak [15]. Jasno je, da sta vnetna stanja in imunski status bolnikov ključnega pomena pri določanju poteka napredovanja bolezni [12]. Umrli med bolniki s COVID-19 so pokazali močno povezavo s starostjo [1]. Skupina, stara 30 let ali manj, je imela manj smrtnosti, medtem ko je skupina, stara 65 let ali več, pokazala dramatično visoko smrtnost (Data.CDC.gov). V večini držav so opazili več smrti pri okuženih moških kot pri okuženih ženskah [16]. Višjo smrtnost zaradi COVID-19 so opazili tudi pri kadilcih, debelih posameznikih in bolnikih s kronično ledvično boleznijo, srčno-žilnimi boleznimi ali rakom [17]. Največja sprememba v stopnji umrljivosti je povezana z nedavnim pojavom različice Omicron, ki je visoko prenosljiva z nižjo stopnjo umrljivosti kot pri drugih VoC [18, 19]. Seveda je lahko ta sprememba v stopnji smrtnosti posledica uspeha cepljenja. Dejansko so poročali, da je smrtnost med necepljenimi, zlasti starejšimi od 75 let, še vedno zelo velika [20]. Kot leteči sesalci so netopirji super zodiakalni rezervoar virusov, zlasti koronavirusov. Imajo pa netopirji edinstven imunski sistem, ki je dobro uravnotežen med obrambo in imunsko toleranco, kar jim preprečuje razvoj patoloških sprememb po virusni okužbi. Imajo okrepljeno konstitutivno izražanje interferonov (IFN), genov, stimuliranih z interferonom, in več proteinov toplotnega šoka. Po drugi strani pa imajo netopirji zmanjšan stimulator interferonskih genov (STING) in zatrto pirinsko domeno družine NLR, ki vsebuje 3 (NLRP3) inflamasom [21]. V nasprotju z netopirji ljudje nismo popolnoma odporni na nekatere okužbe s koronavirusom [21]. Zanimivo je omeniti, da je v nasprotju z okužbami z drugimi virusi, kot so črne koze, ošpice ali steklina, izpostavljenost SARS-CoV-2, zlasti z različico Omicron, posameznikov, ki so prejeli cepivo ali preboleli predhodno okužbo. z drugimi različicami lahko povzroči bolezen, vendar z blažjimi simptomi ali brez njih [22]. Takšno izogibanje imunskemu sistemu oteži izločanje virusa. Genetske variacije virusa SARS-CoV-2 so zagotovo glavni dejavnik, ki prispeva k nepopolni imunski zaščiti. Večina dosedanjih del je trdno podpirala idejo, da SARS-CoV-2 ne okuži krvnih levkocitov v obtoku, saj ne izražajo receptorja SARS-CoV-2, angiotenzinske konvertaze 2 (ACE2). Zelo nedavna študija [23] je pokazala, da je lahko do 6 % krvnih monocitov okuženih z virusom, vendar to zahteva nadaljnjo potrditev. Drug pomemben dejavnik je, da mukozna SARSCoV-2 specifična IgM in IgA zelo hitro razpadeta [24]. Možno je tudi, da bi nevtralizacijo virusa lahko dosegli samo s protitelesi, specifičnimi za receptorsko vezavno domeno (RBD), in da je RBD skrit z zvijanjem beljakovin do tik pred vezavo na ACE2 [25].

cistanche tubulosa - izboljšanje imunskega sistema
PRIROJENA IMUNITETA
Številne študije v zadnjih dveh letih so pokazale, da je prirojeni imunski sistem ključni branilec pred SARSCoV-2. V najboljših primerih prirojena imunost odstrani SARS-CoV-2 brez aktivacije adaptivnega imunskega sistema in tako ustvari tako imenovano kohorto »nikoli-COVID«. To idejo močno podpira nedavno uvedena izzivna študija SARS-CoV-2 pri ljudeh (NCT04865237), v kateri so 36 mladim zdravstvenim prostovoljcem intranazalno dajali 10 TCID50 SARS-CoV-2/ človek/GBR/ 484861/2020 (D614G, ki vsebuje pre-alfa divji tip virusa; pristopna številka Genbank OM294022). Presenetljivo je 16 prostovoljcev (~44,4 %) ostalo neokuženih po namerni izpostavljenosti SARS-CoV-2. Njihov C-reaktivni protein (CRP), nevtralizirajoče protitelo SARS-CoV-2 in protitelesa, specifična za konice, ostajajo negativni, pri čemer so izključeni prispevki adaptivnih imunskih celic pri takšni zaščiti [26]. Vendar pa lahko prirojeni imunski branilci postanejo tudi škodljivi, če se neustrezno aktivirajo med okužbami s SARSCoV-2 [27].
CELIČNA PRIROJENA IMUNOST
Genetski dokazi kažejo, da ima celično posredovana prirojena imunost ključno vlogo pri odpornosti na COVID-19 in pri patogenezi hude bolezni [28–30]. Geni, ki igrajo ključno vlogo, vključujejo kemokine in njihove sorodne receptorje ter člane poti IFN. Celični in prirojeni imunski receptorji, ki prepoznajo SARS-CoV-2, spadajo v različne razrede [31]. Genetski podatki o miših in ljudeh nedvoumno dokazujejo, da zaporedja RNA, bogata z GU, prepozna Toll-like receptor 7 (TLR7) v plazmocitoidnih dendritičnih celicah (pDC) in TLR8 v običajnih DC in mieloidnih celicah [32]. Ti receptorji TLR se nahajajo v endosomskem predelu in sprožijo proizvodnjo IFN (pDC), predstavitev antigena in nenadzorovano vnetje v poznejših fazah. V skladu s temi podatki in vitro in in vivo pri miših je bila genetska pomanjkljivost TLR7 povezana s hudo boleznijo [33]. Domneva se tudi, da citosolni receptorji, vključno s kompleksom gena -1 (RIG-1), inducibilnega z retinojsko kislino, zaznavajo nukleinske kisline SARS-CoV-2 [31]. Nedavni dokazi kažejo, da površinski lektini tipa C medsebojno delujejo z glikozidnimi komponentami konice in igrajo pomembno vlogo pri vstopu virusa [34–37]. Provnetni makrofagi so glavna vrsta imunskih celic, ki izražajo visoke ravni ACE2 [38]. Po okužbi s SARS-CoV-2 ti makrofagi sproščajo vnetne citokine in kemokine, vključno s kemokinskim ligandom 7 (CCL7), CCL8 in CCL13 motiva CC, da rekrutirajo in aktivirajo celice T. Celice T pa proizvajajo IFN- in druge citokine za nadaljnjo aktivacijo makrofagov [39]. Ta pozitivna povratna zanka spodbuja dvig in nadaljevanje patološkega vnetja. Epidemiološki podatki kažejo, da so starejši odrasli in ljudje z osnovnimi zdravstvenimi težavami pokazali izjemno visoko stopnjo hudih bolezni in umrljivosti [17]. Skupaj s staranjem obstaja težnja po povečanju vnetnih makrofagov [40]. To ne pojasnjuje le, zakaj je pojav kroničnih vnetnih bolezni bolj razširjen, ampak tudi daje možnost, da pojasni visoko incidenco hudih primerov COVID-19 pri starejših ljudeh. Poleg tega scenarija je razumno razumeti, zakaj je okužba s SARS-CoV-2 pri tistih z osnovnimi zdravstvenimi težavami pokazala tudi večjo razširjenost hudih bolezni in umrljivosti [12]. Enocelično sekvenciranje v kombinaciji s citometrijo po času letenja (CyTOF), Cite-Sequencing ali večbarvna sosednja citometrija je bilo še posebej informativno pri opisovanju odstopanj prirojenih imunskih celic pri bolnikih s COVID-19. Na začetku je bilo dokazano, da so bili granulociti in monociti dramatično spremenjeni pri bolnikih s hudim potekom bolezni, medtem ko so zmerni in blagi poteki bolezni pokazali precej redne programe aktivacije vnetnih celic z visoko stopnjo izražanja humanega levkocitnega antigena-DR (HLA-DR) in CD11c [ 27]. Pri hudi bolezni COVID-19 je za monocite značilna visoka raven izražanja alarminov in CD163, medtem ko so molekule glavnega histokompatibilnega kompleksa (MHC) zmanjšane. Znotraj nevtrofilnega predela so pri hudi bolezni COVID-19 opažena celična stanja, ki spominjajo na celice, podobne supresorjem, ki izhajajo iz mieloidov, hkrati pa so prekomerno izraženi celični programi, potrebni za tvorbo zunajceličnih pasti nevtrofilcev (NET). Poleg tega je pojav prekurzorjev nevtrofilcev v krvi očiten za nujno mielopoezo pri bolnikih s hudo boleznijo COVID-19. Mononuklearni fagociti so izjemno plastični in raznoliki ter so podvrženi različnim oblikam aktivacije in tolerance [41, 42]. Funkcija makrofagov ima prilagoditveno komponento, ki se imenuje "usposabljanje". Izurjena prirojena imunost je osnova za zaščito pred patogeni, povezano z izbranimi cepivi, okužbami in citokini, kot je interlevkin-1 (IL-1) [43]. Obstajajo dokazi, da lahko usposobljena prirojena imunost prispeva k odpornosti proti COVID-19. Na primer, če so bile matere zaradi cepljenja posredno izpostavljene živemu cepivu proti otroški paralizi, je bilo ugotovljeno, da imajo njihovi otroci zmanjšano simptomatsko okužbo s COVID-19 [44]. Pomen usposobljene prirojene imunosti na COVID-19 in na cepiva, ki se trenutno uporabljajo, je treba še opredeliti. Glavna klinična težava hudega COVID-19 je razvoj "sindroma akutne dihalne stiske" (ARDS), povezanega s podaljšano respiratorno odpovedjo in visoko smrtnostjo. Tudi tu so prirojene imunske celice povezane s to patofiziološko reakcijo pri hudi bolezni COVID-19 [45]. Pri bolnikih z ARDS se kopičijo makrofagi iz monocitov, ki izražajo CD163- in so pridobili profifibrotični transkripcijski fenotip [45]. Profibrotični programi pljučnih makrofagov pri COVID-19 spominjajo na celično reprogramiranje, ki je bilo prej ugotovljeno pri idiopatski pljučni fibrozi. Presenetljivo je, da je in vitro izpostavljenost monocitov SARS-CoV-2 v zadostni meri povzročila takšen profifibrotični fenotip [45]. Pri COVID-19 so spremenjene tudi druge prirojene imunske celice [46]. Na primer, pri hudih bolnikih s COVID-19 so celice Nature killer (NK) pokazale podaljšano izražanje genov, ki jih spodbuja IFN (ISG), medtem ko so gene, ki jih povzroča faktor nekroze tumorja (TNF), opazili pri blagi in zmerni bolezni. Poleg tega so celice NK pri hudi bolezni COVID-19 pokazale oslabljeno delovanje proti celicam, okuženim s SARS-CoV-2, in oslabljeno antifibrotično delovanje [46]. Druge študije so pokazale, da prezgodnji odzivi transformirajočega rastnega faktorja (TFG) omejujejo protivirusne funkcije NK celic pri hudi bolezni [47]. Presenetljivo je bilo tudi za druge celice, pridobljene iz krvi, vključno z megakariociti in eritroidnimi celicami, značilno povečano izražanje ISG pri hudem, a ne blagem COVID-19, kar dodatno podpira podaljšan odziv IFN, ki je neposredno povezan z resnostjo bolezni [48]. Poleg tega se zdi, da SARS-CoV-2 sproži prirojeno delovanje v podmnožici celic T, in sicer visoko aktiviranih celicah T CD16+, ki se pojavljajo predvsem pri hudi bolezni COVID-19 v CD4, CD8 in δ celice T [49]. Dokazano je bilo, da je povečano nastajanje C3a pri hudi bolezni COVID-19 povzročilo ta nenavaden fenotip celic T. Funkcionalno je CD16 omogočil z imunskim kompleksom posredovano, od T-celičnega receptorja (TCR) neodvisno degranulacijo in citotoksičnost, ki se doslej zdi specifična za SARS-CoV-2.
Te funkcije so bile nadalje povezane s sproščanjem kemoatraktantov nevtrofilcev in monocitov ter poškodbo mikrovaskularnih endotelijskih celic, pri čemer so slednje odgovorne za heterogene in raznolike klinične simptome, ki vključujejo veliko različnih organov pri hudi bolezni COVID{0}}. Skrb vzbujajoče je obstojnost citotoksičnega fenotipa klonov T celic CD16+ tudi po akutni bolezni, ki je prav tako lahko vpletena v patofiziološke mehanizme, povezane z dolgotrajno boleznijo COVID. Vendar to očitno zahteva nadaljnje preiskave. Zdi se, da prirojena funkcionalnost celic CD16+ T nima le pomembne patofiziološke vloge, ampak se je pokazalo, da je delež teh celic skupaj s plazemskimi nivoji proteinov komplementa pred C3a povezan s smrtnimi izidi.

koristi dodatka cistanche-povečanje imunosti
Kliknite tukaj za ogled izdelkov Cistanche Enhance Imunity
【Vprašajte za več】 E-pošta:cindy.xue@wecistanche.com/Whats App: 0086 18599088692/Wechat: 18599088692
HUMORALNI PRIROJENI IMUNSKI ODZIV NA OKUŽBO SARS-COV-2
Prirojena imunost je sestavljena iz celičnega in humoralnega kraka [50]. Komponente humoralne veje prirojene imunosti so raznovrstni nizi molekul, kot so komponente komplementa, zbirke (npr. lektin, ki veže manozo, MBL), fikolini in pentraksini (npr. C reaktivni protein, CRP in PTX3) [50]. , 51]. Te molekule za prepoznavanje vzorcev tekoče faze imajo podobne funkcije kot protitelesa (avtoprotitelesa). Med temi protitelesi je bilo ugotovljeno, da MBL veže konico s prepoznavanjem svojih glikozidnih delov in zavira SARSCoV-2 [36]. MBL je prepoznal vse VoC, vključno z Omicronom. Ugotovljeno je bilo, da so haplotipi MBL povezani z resnostjo bolezni [36]. Pentraksin 3 (PTX3), vendar ne njegov daljni sorodnik CRP, je vezal nukleoprotein SARS-CoV-2, vendar je treba še pojasniti, ali njegovo prepoznavanje okrepi vnetje [36]. Dejansko se je PTX3 izkazal kot pomemben biomarker resnosti bolezni z na primer smrtjo kot končno točko [52–56]. Rezultati so bili razširjeni na dolgi COVID [57], pri čemer je PTX3 del podpisa resnosti bolezni. Komplement se je pojavil kot pot ojačanja vnetja in poškodbe tkiva [58]. Pot lektina lahko igra vlogo pri aktivaciji komplementa. Majhne pilotne študije kažejo, da je lahko ciljanje komplementa z zaviranjem C3 konvertaze ali z blokiranjem z manozo povezane serinske proteaze (MASP) in lektinske poti koristno pri COVID-19 [49, 59–63]. Ali lahko ti terapevtski pristopi vplivajo tudi na funkcionalnost visoko aktiviranih celic CD16+ T s prirojeno imunsko funkcijo, je potrebna nadaljnja preiskava [49]. Tako ima humoralna prirojena imunost (ante-protitelesa) pomembno vlogo pri COVID-19. MBL predstavlja neredundantno pot odpornosti proti SARS-CoV-2 VoC. Pentraksina CRP in PTX3 zagotavljata pomembne prognostične indikatorje, pri čemer PTX3 vključuje aktivacijo mieloidnih celic in endotelijskih celic. Pomembno bo nadalje raziskati vrednost in pomen ante protiteles kot biomarkerjev (PTX3), kandidatov za zdravljenje (MBL) in terapevtskih ciljev (komplement). Makrofagi in monociti izražajo različne receptorje za prepoznavanje vzorcev (PRR), vključno s TLR, (NOD) podobnimi proteini družine receptorjev (NLR), ki jih ni pri melanomu 2 (AIM2) in poti ciklične GMP-AMP sintaze (cGAS)-STING. Ti lahko sprožijo prirojene imunske odzive na virusno okužbo z neposredno okužbo in zaznavanjem SARS-CoV-2 ali z odkrivanjem molekularnih vzorcev, povezanih s poškodbami (DAMP) ali molekularnih vzorcev, povezanih s patogeni (PAMP), ki jih sproščajo okužene celice, ki delujejo kot mehanizem za naprej, ki širi sistemski vnetni odziv. Enocelično sekvenciranje in druge citometrične analize so ugotovile prisotnost SARS-CoV-2 RNA v človeških pljučnih makrofagih [30, 39] in krvnih monocitih [64]. Niti človeški pljučni makrofagi niti monociti ne izražajo primarnega internalizacijskega receptorja SARS-CoV-2- 2 ACE2, zato so bili predlagani alternativni mehanizmi za internalizacijo virusa, vključno s prevzemom, ki ga posreduje Fcreceptor [23, 65]. Pljučne mieloidne celice, okužene s SARS-CoV-2, inducirajo transkripcijske programe in signalne kaskade prirojenega imunskega odziva. Celice, okužene s SARS-CoV-2-, uravnavajo kemokine, citokine, pot IFN in gene, povezane s TNF [30, 39]. Ti delujejo tako, da zavirajo širjenje virusa in rekrutirajo monocite in celice T na mesto okužbe. Vendar pa so čezmerno sproščanje protivnetnih citokinov zgodaj ugotovili pri bolnikih s hudim COVID-19 [66]. Odkrivanje virusne RNK potencialno spodbuja aktivacijo tega transkripcijskega odziva z endosomskima TLR3 in TLR7, kot tudi zaznavanje SARS-CoV-2 E proteina na celični membrani s TLR2 [67]. Nedavna poročila so pokazala prisotnost z oligomerizirano apoptozo povezano pegasto beljakovino, ki poleg NLRP3 vsebuje domeno za aktiviranje in rekrutiranje kaspaze (CARD) v monocitih in pljučnih makrofagih bolnikov s COVID-19 [68]. Monociti so pokazali sočasno aktivacijo kaspaze-1 ter cepitev in translokacijo kompleksa por gastrina D na plazemsko membrano, spodnji dogodek aktivacije inflamasoma, ki olajša sproščanje citokinov in je pred procesom vnetne litične celične smrti, znane kot piroptoza . Dejansko so serumi bolnikov s COVID-19 obogateni za IL-1, IL-18 in laktat dehidrogenazo (LDH), kar kaže na trenutno piroptozo [68]. V pljučih posameznikov s COVID-19 vnetna aktivacija ni izključno samo celic, okuženih s SARS-CoV-2-, kar nakazuje, da lahko parakrini signali, ki jih povzroči okužba s SARS-CoV-2, povzročijo piroptozo v sosednjih celicah , ki potencira vnetni odziv in resnost bolezni [64]. Inhibitorji, ki ciljajo na komponente vnetne poti, vključno s kaspazo-1 in NLRP3, so zmanjšali patologijo v humaniziranem mišjem modelu okužbe s SARS-CoV-2 [65], kar kaže na to, da lahko terapevtsko ciljanje na vnetje NLRP3 zagotovi translacijske koristi, ko družba napreduje živeti ob SARSCoV-2. Vendar je pomembno upoštevati, da se večina študij na ljudeh opira na posmrtna tkiva in zato predstavlja najhujšo obliko bolezni. Posledično je treba še ugotoviti, ali lahko inhibicija inflammasoma prinese učinkovite rezultate pri blagih oblikah COVID-19. Prirojeni imunski odziv na okužbo s SARS-CoV-2 ni omejen na makrofage in monocite in je pogosto povezan z nenormalno aktivacijo in rekrutiranjem nevtrofilcev. Poročali so o dramatičnem povečanju mieloičnemu supresorju podobnih celic (podobnih MDSC) [69], zlasti pri tistih v hudih fazah COVID-19, kar prispeva k patogenezi SARS-CoV{ {106}} okužba. MDSC lahko upočasnijo očistek virusa SARS-CoV-2 ter zavirajo proliferacijo in delovanje celic T. Znano je, da nevtrofilci sproščajo NET in neravnovesje med tvorbo in razgradnjo NET ima osrednjo vlogo v patofiziologiji z lovljenjem vnetnih celic in preprečevanjem pridobivanja celic, ki popravljajo tkiva. Strategije, ki neregulirajo tvorbo NET ali uničijo NET z sredstvi, kot je DNaza, bi lahko predstavljale nove terapije za bolnike s COVID-19, zlasti tiste s hudo boleznijo [2], glejte spodaj.
VASKULARNE OKLUZIJE, KI JIH POGNAJO MREŽA, POGONIJO PATOLOGIJO PRI HUDI COVID-19-19
Med raztrganjem membrane granulocitov v procesu tvorbe NET se predhodno oblikovani provnetni citokini (npr. IL-6) in kemokini (npr. IL-8, CCL3) ter protimikrobni peptidi (npr. baktericidne beljakovine in histoni, ki povečujejo prepustnost), serinske proteaze (npr. nevtrofilna elastaza in proteinaza 3), drugi encimi (npr. mieloperoksidaza, laktoferin, lizocim in fosfolipaza A2) in reaktivne kisikove spojine (ROS) se sproščajo v bližino od NET. Dejavnost topnih mediatorjev zbledi, ko se NET, ki nastane pri visoki gostoti nevtrofilcev, nagiba k agregaciji. Ti agregati delujejo protivnetno, saj proteaze, ki se prenašajo z NET, proteolitično razgradijo vnetne mediatorje in toksične histone [70, 71]. Pomembno je, da proteaze, vezane na DNA, niso antagonizirane z antiproteazami [72]. Tako nastanek NET velja za dvorezen meč, ki sprva sproži vnetje in kasneje pomaga orkestrirati njegovo razrešitev. Neravnovesje med tvorbo in razgradnjo NET lahko povzroči tudi vnetje, npr. z zamašitvijo žil in kanalov [73]. Prva poročila o vlogi NET pri bolnikih s COVID-19 so bila objavljena že kmalu po začetku pandemije in opisujejo povišane ravni označevalcev NET, kot so brezcelična DNK, citrulinirani histon H3 (citH3) in mieloperoksidazna DNK (MPO-DNA) kompleksov v serumih teh bolnikov [74]. Enocelično sekvenciranje krvno pridobljenih nevtrofilcev iz periferne krvi je podprlo reprogramiranje podskupine nevtrofilcev v smeri transkripcijskih programov, povezanih s tvorbo NET, zlasti pri hudi bolezni COVID-19 [27]. Serum bolnikov s COVID-19 kot tudi sam virus naj bi lahko sprožila tvorbo NET, ki jo spremljajo naraščajoče ravni znotrajceličnega ROS [74–76]. Ta pot ROS-NET skupaj z aktivacijo nevtrofilcev, tvorbo nevtrofilnih trombocitnih agregatov in intravaskularno agregacijo NET, obogatenega s komplementom in tkivnimi faktorji, tvori okluzivne imunske tromboze, ki izvirajo iz NET, slika 2. To je še posebej nevarno v mikrovaskulaturi, kjer pride do hudih poškodb organov zaradi motene mikrocirkulacije [72, 77–79]. Zaradi svoje osrednje vloge v patofiziologiji COVID-19 je NET glavna tarča za terapevtsko posredovanje. Pokazalo se je, da terapevtski odmerki heparina preprečujejo agregacijo NET z nano- in mikrodelci, učinkovitost te terapije pri bolnikih s COVID-19 pa je bila nedavno prikazana [80, 81]. Poleg tega je znano, da heparin pospeši razgradnjo NET, posredovano z DNazo I, in opravljeni so bili prvi poskusi z Dornazo Alfa, rekombinantno DNazo [82, 83]. Disulfiram naj bi bil tudi uspešen pri zmanjšanju NET, povečanju preživetja in izboljšanju oksigenacije krvi na živalskih modelih, zaradi česar je nov obetaven kandidat za zdravljenje z NET povezanih patologij pri bolnikih s COVID-19 [84 ]. Nazadnje se o zaviralcih peptidil-arginin deiminaz (PAD) razpravlja kot o terapijah za zdravljenje z NET povezanih trombotičnih zapletov pri bolnikih s COVID-19, vendar še ni bilo opravljenega nobenega kliničnega preskušanja [85].

Slika 2 NEToza. Imunska fluorescenca zazna komponente NET, citrulinirane Histon H3 in nevtrofilno elastazo (oboje zeleno) ter ekstranuklearno DNA (DAPI; rdeče) v žilah osrednjih človeških pljuč. Upoštevajte, da intravaskularni kompleksi DNA-encim-histoni napolnijo celoten lumen številnih žil (nekatere zamašene žile so označene z zvezdicami).
CILJANJE NA PROIZVODNJO IFN TIPA I S SARS-COV-2
Medtem ko prirojena imunost predstavlja prvo linijo obrambe gostitelja pred virusno okužbo, je odziv IFN tipa I jedro, ki daje protivirusne aktivnosti gostiteljskim celicam, kar je sestavljeno iz dveh glavnih zaporednih korakov, vključno s proizvodnjo IFN in izražanjem ISG [{{1 }}]. Tukaj se posebej osredotočamo na regulacijo proizvodnje IFN tipa I, ki je prvi in kritični korak za učinkovit prirojeni imunski odziv in je zato primarno tarča proteinov SARS-CoV-2 za zatiranje.
Kot je prikazano na sliki 3, se proizvodnja interferona tipa I sproži s prepoznavanjem dvoverižne RNA (dsRNA), ki jo med življenjskim ciklom virusa ustvarijo RIG-1-podobni receptorji (RLR), vključno z RIG -1 in/ali gen za diferenciacijo melanoma 5 (MDA5) v citoplazmi ali TLR v endosomu [87]. Po nalaganju z dsRNA lahko RIG-1 in MDA5 interagirata z adapterskim mitohondrijskim protivirusnim signalnim proteinom (MAVS), kar vodi do tvorbe signalnega kompleksa, ki ga sestavljata TANK vezavna kinaza 1 (TBK1) in inducibilna IκB kinaza (IKKi) . Kompleks TBK1/IKKi nato fosforilira interferonski regulacijski faktor 3/7 (IRF3/7), s čimer spodbuja njihovo translokacijo v jedro, da spodbudi ekspresijo IFN-/. Medtem bi lahko TLR-ji, kot je TLR3, prav tako prepoznali PAMP-je v endosomu, da inducirajo proizvodnjo citokinov in kemokinov, kar poveča prirojeni imunski odziv [87].
Med tem procesom so poročali, da SARS-CoV-2 kodira vsaj 14 proteinov, kar predstavlja približno polovico vseh proteinov, ki jih kodira virus, da moti proizvodnjo IFN [88–90]. Ti proteini vključujejo strukturno membrano (M), proteine nukleokapsida (N), pomožne proteine (3, 6, 8 in 9b) in nestrukturne proteine (NSP1, 3, 5, 6, 12, 13, 14 in 15), ustvarjen iz velikega odprtega bralnega okvirja (ORF), ki kodira 1ab s cepitvijo, ki jo posreduje papainu podobna proteinaza (NSP3, NLpro) in 3C-podobna proteinaza (NSP5, 3CLpro). Zatiranje proizvodnje IFN s proteini SARS-CoV-2 je bilo primarno izvedeno prek štirih vrst mehanizmov, vključno z izogibanjem prepoznavanju virusne RNA (z N, ORF9b, NSP1 in NLpro), ogrožanjem RIG-1 ali TLR signaliziranje (z M, N, 3CLpro, NSP12, ORF3b, ORF6, ORF7b in ORF9b), ciljanje na kompleks TBK1 (z M, N, NSP13, ORF9b,) in motenje aktivacije IRF3 (z M, N, NLpro, 3CLpro, NSP1, NSP12–15, ORF3b, ORF6 in ORF8), sl. 3. V skladu z obsežno motnjo proizvodnje IFN s proteini, kodiranimi s SARS-CoV-2-, so bolniki s COVID-19 običajno pokazali zakasnjen odziv IFN tipa I [90], tj. proizvodnja IFN je bila zavrta v zgodnji fazi okužbe s SARS-CoV-2, kar virusu omogoča uspešno replikacijo v gostiteljskih celicah in spodkopava asimptomatsko okužbo. Izkazalo se je, da izboljšanje odziva IFN na tej stopnji pomaga omejiti okužbo s SARS-CoV-2 [91–93].

koristi cistanche za moške - krepitev imunskega sistema
Po latentnem odzivu IFN so bolniki s COVID-19, zlasti tisti v hudih oblikah, pokazali precej pretiran odziv IFN, ki se je kazal z nenadzorovanim viharjem citokinov in vnetjem, kar ustreza drugemu kraku zapoznelega odziva IFN tipa I pri pozni fazi [90], ki jo osvetljujejo novejše študije. Zhao et al. poročali, da je lahko dvojna vloga strukturnega proteina N, ki temelji na ravni ekspresije, delno odgovorna za aktivacijo signalizacije IFN, kjer je nizek odmerek proteina N supresiven, medtem ko je bil visok odmerek spodbujajoč. To se je izkazalo z dvojno regulacijo fosforilacije in jedrske translokacije IRF3 [94]. Alternativno Ren et al. ugotovili, da lahko SARS-CoV-2 nepričakovano aktivira odziv IFN prek signalne poti cGAS-STING, ki je bila inducirana s citoplazemskimi mikronukleusi, proizvedenimi v večjedrnem sinciciju med celicami, ki izražajo konico in ACE2 [95]. Rezultate so nadalje neodvisno potrdili Zhou et al., ki so dokazali, da je zlitje celica-celica zadostovalo za induciranje citoplazemskega kromatina in pot citoplazemskega kromatina-cGAS-STING, ne pa poti zaznavanja virusne RNA, ki jo posreduje MAVS, prispeva k interferonu in izražanje proinflamatornih genov pri fuziji celic [96]. Zanimivo je, da je več proteinov SARS-CoV-2 (3CLpro, ORF3a in ORF9) prav tako uspelo ciljati na STING za uravnavanje odziva IFN [97], kar verjetno kaže na kompleksno povratno interakcijo med SARSCoV-2 in prirojeno imunost, zato je za zdravljenje COVID-19 potrebna dobro uravnotežena imunska interferenca, usmerjena v odziv IFN.

Slika 3 Ciljanje na proizvodnjo IFN tipa I s SARS-CoV-2. Shematski prikaz virusnih proteinov. Poročali so, da tisti, označeni z zvezdicami, uravnavajo proizvodnjo IFN. b Signalne poti produkcije IFN, na katere ciljajo proteini SARS-CoV-2. Okužba s SARS-CoV-2 inducira zapozneli odziv IFN tipa I, ki je podprt z inhibiranim signaliziranjem RIG-I/MDAS-MAVS v zgodnji fazi in signalizacijo cGAS-STING, aktivirano s citoplazmatskimi mikronukleusi, v pozni fazi .
PRILAGODLJIVA IMUNOST: HUMORALNA IMUNOST NA SARS-COV-2
Prilagodljiva imunost zagotavlja imunost, specifično za patogen, ki izkorenini okužbo in zagotavlja dolg spomin in priklic imunskih odzivov, slika 4. S proizvodnjo protiteles imajo celice B ključno vlogo pri protivirusni imunosti. Različni razredi protiteles, kot so IgM, IgA, IgG in IgE, sodelujejo pri humoralnih imunskih odzivih na virusne okužbe. Za te razrede protiteles so značilne njihove intrinzične lastnosti, funkcije, porazdelitev v tkivih in razpolovne dobe. Po okužbi s SARS-CoV-2 ali cepljenju sta IgD in IgM prva proizvedena tipa protiteles. Pozitiven test protiteles IgM kaže, da je lahko virus prisoten ali da je bolnik pred kratkim okreval po okužbi in da se je začel specifični imunski odziv virusa [98]. Med okužbo s SARS-CoV-2 se simptomi začnejo okoli 5. dne in telo začne proizvajati protitelesa IgM približno 7–8 dni po okužbi [99]. Zaradi nezadostnega zorenja afinitete imajo protitelesa IgM razmeroma nizko afiniteto v primerjavi z IgG. Po drugi strani pa imajo protitelesa IgM zaradi svoje pentamerne narave visoko avidnost za antigene in igrajo ključno vlogo pri opsonizaciji.
Protitelesa IgG se običajno pojavijo pozneje med imunskim odzivom zaradi časa, ki je potreben, da njihova afiniteta dozori, da pridobijo visoko avidnost in močnejšo sposobnost nevtralizacije patogenov, aktiviranja poti komplementa in ubijanja okuženih celic s celično citotoksičnostjo, odvisno od protiteles (ADCC). Protitelesa IgG imajo relativno dolgo razpolovno dobo v serumu in so povezana s spominom celic B. Protitelesa IgG proti SARS-CoV-2 se razvijejo šele približno 14 dni po okužbi [100]. Pozitiven test za IgG je dober znak, da ste bili okuženi ali cepljeni. Zanimivo je, da so med okuženimi s SARS-CoV-2 zaznavna protitelesa IgG večinoma IgG1 in IgG3 [101]. Protitelesa IgA nastajajo takoj za IgM s serumskimi ravnmi, višjimi od IgM, in so glavni razred protiteles na površinah sluznice in izločkih. Poročali so, da je IgA, specifičen za SARS-CoV-2-, mogoče odkriti pred pojavom IgM in prevladuje v zgodnjih nevtralizirajočih odzivih [102]. IgA ob izločanju tvori dimere za povečanje avidnosti. Protitelesa IgA, ki se izločajo v dihalni trakt, igrajo ključno vlogo pri imunosti sluznice na okužbo s SARSCoV-2, tako da olajšajo agregacijo in preprečijo začetno okužbo gostiteljskih celic. Pomembno je omeniti, da zaznavne ravni nevtralizirajočih protiteles proti SARS-CoV-2 začnejo upadati v treh mesecih po blagih in asimptomatskih okužbah. To lahko napoveduje prehodno imunost in povečano tveganje za ponovno okužbo. Zanimivo je, da je več skupin poročalo o jasni povezavi med obsegom T-celične imunosti in humoralnim odzivom pri rekonvalescentih [103–105]. Ugotovljeno je bilo, da imajo bolniki s hudim COVID-19 nizke frekvence mutacij v svojih genih spremenljivih regij težke verige v prvih tednih po okužbi, predvsem v tistih protitelesih proti proteinu spike [106], kar kaže na suboptimalno zorenje imunoglobulina. Poleg tega so pri hudih oblikah v primerjavi z blažjimi oblikami COVID-19 opazili tudi zamudo pri pojavu protiteles, vključno z nevtralizirajočimi protitelesi proti SARSCoV-2 [107, 108]. To je v skladu z dejstvom, da so celice CD4+ T bistvene za vzdrževanje tvorbe zarodnega središča (GC) in diferenciacije celic B, ki vodi do zamenjave izotipa in zorenja imunoglobulina, kar sta dve značilnosti humoralnega odziva, odvisnega od celic T. Dosledno je okvarjena tvorba GC povezana z izčrpanostjo celic T CD4+ v bezgavkah bolnikov s hudim COVID-19 [109]. Ta okvara in zamuda pri razvoju protiteles proti spike proteinu lahko prispevata k širjenju virusa in daljši obstojnosti SARS-CoV-2 pri bolnikih [110]. Poleg tega je bilo prezgodnje izčrpavanje T-celic zaradi apoptoze povezano z nižjim odzivom B-celic pri posameznikih, okuženih s filovirusom [111] ali retrovirusom [112, 113]. V kolikšni meri je smrt celic CD4+ T zaradi apoptoze [114] lahko povezana z zamudo pri vzpostavljanju učinkovitega humoralnega odziva in pri razvoju posledic, si zasluži nadaljnjo preiskavo.

rastlina cistanche krepi imunski sistem
PRILAGODLJIVA IMUNOST: CELIČNA IMUNOST IN ODPORNOST NA SARS-COV-2
Specifično celično imunost na SARS-CoV-2 posredujejo celice T. Te celice so naivne in krožijo v krvnem obtoku in perifernih limfoidnih organih, dokler ne naletijo na svoj specifični antigenski peptid, ki ga predstavi MHC. Sam virus SARS-CoV-2 ali goli virusni peptidi niso mogli aktivirati celic T. Interakcija z visoko afiniteto med samopredstavljenimi MHC peptidi SARS-CoV-2 in TCR inducira proliferacijo in diferenciacijo celic T v celice, ki lahko prispevajo k odstranitvi z virusom okuženih celic ali pomagajo pri nastajanju protiteles. MHC razreda I predstavlja endogene antigene peptide, ki aktivirajo CD8+ T celice, medtem ko razred II MHC predstavlja eksogene antigene peptide, ki aktivirajo CD4+ T celice. Specifične celice T za SARS-CoV-2 so ključne za imunost proti okužbam in poročali so, da je dovzetnost za hudo bolezen povezana z aleli HLA [115]. Znano je, da vnetni monociti in makrofagi ter DC izražajo ACE2, ki omogoča vstop SARS-CoV-2 v te profesionalne celice, ki predstavljajo antigene, da aktivira T-celice, zlasti CD8+ T-celice. Čeprav je izražanje ACE2 na makrofagih in DC le na vmesnih ravneh, lahko sočasno izražanje CD209 (DC-SIGN) močno olajša vstop SARS-CoV-2 v DC [116]. Treba je poudariti, da v večini primerov okužbe s SARS-CoV-2 ne izzovejo dramatičnega vnetnega odziva v makrofagih in DC. IL-6 skoraj ni mogoče zaznati, drugi citokini, kot je IL-1, pa so zelo nizki [117]. To lahko omeji njihovo migracijo v lokalno limfoidno tkivo in zorenje v celice z izražanjem kostimulacijskih molekul, ki so zelo učinkovite pri predstavitvi antigena celicam T v obtoku, kar kaže, da je močan odziv celic T na SARS-CoV-2 morda težko doseči. inducirajo in s tem omejijo razvoj imunosti. Pomembno je omeniti, da lahko celice B služijo tudi kot celice, ki predstavljajo antigen SARS-CoV-2, zlasti tiste s površinskim imunoglobulinom, specifičnim za antigene SARS-CoV-2. Bolniki s COVID-19 v hudi fazi so se kazali z zmanjšanimi perifernimi limfociti, imenovanimi limfopenija ali limfocitopenija, za katere se domneva, da spodbujajo napredovanje bolezni [118]. Ker limfociti komajda izražajo ACE2, je malo verjetno, da bi bil neposredna tarča virusa SARS-CoV-2 [119]. Za izgubo limfocitov sta bila predlagana dva glavna posredna mehanizma. Ena je povečana celično avtonomna smrt, predvsem z apoptozo. Celice T, izolirane pri bolnikih s hudo boleznijo COVID-19, so pokazale povečano nagnjenost k smrti zaradi apoptoze, kar dokazuje višja raven aktivacije kaspaze in izpostavljenosti fosfatidilserinu ter visoka stopnja spontane apoptoze [114]. To je bilo močno povezano s povečano količino topnega liganda Fas v serumih in s povečano ekspresijo Fas/CD95 na celicah T, zlasti na celicah T CD4+ [114, 120]. Čeprav je bilo ugotovljeno, da sta vpleteni tako zunanja kot intrinzična apoptoza, ne pa tudi nekroptoza, je zdravljenje s Q-VD, zaviralcem pan-kaspaze, zaščitilo izolirane celice T pred celično smrtjo in povečalo izražanje transkriptov Th1 [114]. Dosledno je bilo ugotovljeno, da sta TNF- in IFN- izrazito povečana v serumih bolnikov s hudim COVID-19, kar je bilo povezano s pojavom, imenovanim citokinska nevihta ali virusna sepsa [31]. Ta pojav je vsaj delno povzročen z vnetno celično smrtjo PANoptoza, skrajšano za mešano celično smrt piroptoze, apoptoze in nekroptoze. Pomembno je, da se je smrtnost, ki jo povzroči TNF-/IFN- -pri živalih, lahko rešilo skupaj s povečano ravnjo celic T pri miših Ripk3‒/‒ Casp8‒/‒, pri katerih je bila PAnoptoza potlačena [121]. Drug mehanizem, odgovoren za izgubo limfocitov, neavtonomno posreduje sincicij, ki bi ga lahko učinkovito induciral SARS-CoV-2 prek njegovega fuzogenega spike proteina, ki ga narekuje vdelan bi-argininski motiv [122]. Ugotovljeno je bilo, da lahko večjedrni sincicij internalizira infiltrirane žive limfocite, prednostno celice CD8+ T, da tvorijo strukture celice v celici, kar je edinstven pojav, ki prevladuje v tumorskih tkivih [123] in igra pomembno vlogo. pri klonski selekciji in imunski homeostazi in podobno [124–126]. Privzeto, kot se dogaja v rakavih celicah, je tvorba strukture celica v celici v prvi vrsti povzročila smrt internaliziranih limfocitov znotraj sincicija, kar je vodilo do hitre eliminacije, ki jo je bilo mogoče rešiti z blokiranjem tvorbe sincicija ali celične celično posredovano smrtjo in tako zagotavlja novo tarčo za zdravljenje COVID-19 [127–130]. Zanimivo je, da se zdi, da oba mehanizma limfopenije dajeta prednost ciljnim limfocitom, pri čemer je avtonomni za CD4+ T celice, medtem ko je neavtonomni za CD8+ T celice [114, 122], ali prednost velja tudi za druge vrste limfocitov in njegove biološke lastnosti ter morebitne posledice zahtevajo nadaljnje preiskave. Poleg neposrednega uravnavanja celičnosti limfocitov je bilo pred kratkim dokazano, da sincicij lahko aktivira signalizacijo cGAS-STING z indukcijo golih citoplazemskih mikronukleusov [95, 96] in sproži vnetno celično smrt [131], oboje pa čeprav bi lahko pomagal vzpostaviti imunost proti okužbam, bi sčasoma spodbudil vnetje in poškodbe tkiva, ki vodijo v hujša klinična stanja. Po naključju je manj patogena različica Omicron SARS-CoV-2 pokazala ogroženo sposobnost induciranja tvorbe sincicija v celicah, ki izražajo človeški ACE2 [132–134]. Skupaj lahko sincicij in različne vrste celične smrti služijo kot pomembno vozlišče za patogenezo, ki jo povzroči okužba s SARS-CoV-2. Čeprav je splošno priznano, da ima T-celična imunost osrednjo vlogo pri nadzoru SARS-CoV-2, je njen pomen še vedno podcenjen in mehanično nejasen. Ustrezen odziv T-celic je pomemben za omejitev okužbe. Za razliko od protiteles, ki so manj obstojna in jih lahko nevtralizirajo samo tista, ki so specifična za RBD, celice T reagirajo na vsaj 30 epitopov virusnih proteinov in izkazujejo trajen spomin. Da so CD{105}} T celice bolj nagnjene k apoptozi, lahko prispeva tudi k razvoju "nemočnih" CD{106}} T celic, ki so izčrpane in krajše živeče celice [135, 136], kar vodi do okvarjena toksičnost T-celic [137] in smrt celic T CD8+ [114] pri bolnikih s hudo boleznijo COVID-19. Poleg tega zgoraj omenjene visoko aktivirane celice T CD16+ prav tako prispevajo k patofiziologiji COVID-19 [49]. Tako bi lahko bilo preprečevanje limfopenije, smrti celic T in neustrezne funkcionalnosti celic T CD16+ zanimivo za omejitev patogenosti in verjetno dolgoročnih posledic. Dosledno je uporaba zaviralcev kaspaze v zgodnji fazi okužbe zagotovila zaščito za opice, pri katerih se razvije sindrom pridobljene imunske pomanjkljivosti (AIDS) [138]. Zato bi lahko bile podobne strategije zanimive za okužbo s SARS-CoV-2. Medtem, čeprav je COVID-19 pri otrocih redko hud, je podskupina bolnikov razvila multisistemski vnetni sindrom pri otrocih z močnimi odzivi na interferon tipa II in NF-kB, kar se kaže s prehodno ekspanzijo celic T TRBV11-2. klonotipi in znaki vnetne T-celične aktivacije [139]. Povezava z aleli HLA A*02, B*35 in C*04 kaže na genetsko nagnjenost, ki jo je treba še potrditi v večjih kohortah [139]. Medtem ko imajo fizični in duševni stresi, bodisi akutni bodisi kronični, dramatičen vpliv na imunski sistem, so lahko prizadete tako prirojene kot adaptivne imunske komponente. Ljudje in živali, izpostavljeni stresnim razmeram, so pokazali znatno zmanjšanje limfocitov [140], povečanje proizvodnje IL-6 [141], zmanjšanje IFN- [142], povečanje regulatornih celic T [142] in sprememba črevesne mikrobiote [143]. Indukcija izražanja Fas na limfocitih s kroničnim stresom [144] bi lahko vsaj delno pojasnila razvoj limfopenije pri zgoraj omenjenih bolnikih s COVID-19. Nujno je treba poudariti, da razširjenosti stresa, povezanega z anksioznostjo, depresijo, strahom in neustrezno socialno podporo med pandemijo COVID-19, ne smemo zanemariti. Obstaja močna potreba po razumevanju vpliva stresa na izkušnje s COVID-19 in obvladovanje stresa bi moralo biti vključeno v oskrbo bolnikov, zlasti tistih z duševnimi in psihičnimi motnjami.

Slika 5 Slika prikazuje SARS-CoV-2 spike protein receptor binding domain (RBD), ki ga vežejo nevtralizirajoča protitelesa razreda 1/2 (modro), razreda 3 (oranžno) in razreda 4 (zeleno). Moč in širina nevtralizacije med različicami SARS-CoV-2 sta označena za vsak razred protiteles [171–173].
TERAPEVTSKO PROTETELESO PROTI SARS-COV-2
Monoklonske snovi živalskega ali človeškega izvora so bile uporabljene za razvoj večine diagnostičnih testov, ki temeljijo na nepolimerazni verižni reakciji (PCR).--. Običajno ciljajo na nukleokapsid, ki je najpogostejši protein virusa. Med pandemijo so jih uporabili v več sto milijonih hitrih testov. Tu se bomo osredotočili na uporabo človeških monoklonskih protiteles (kuhalnice). Pred pandemijo SARS-CoV-2 so se hmAbs pogosto uporabljala za zdravljenje raka ter vnetnih in avtoimunskih bolezni [145]. Z izjemo protitelesa proti respiratornemu sincicijskemu virusu, odobrenega za klinično uporabo leta 1998 [146], se hmAb niso uporabljala za nalezljive bolezni, ker zahtevajo intravensko dajanje velikih količin in so bila predraga v primerjavi s standardom oskrbe pri nalezljivih boleznih. Igra se je začela spreminjati s pionirskim delom, ki ga je opravil Antonio Lanzavecchia med izbruhom SARS-CoV-1 v letih 2002–2003 [147]. Prvič je njegovemu laboratoriju uspelo klonirati iz okrevajočega pacienta protitelo, ki proizvaja celice B in nevtralizira virus. Od takrat so postale na voljo številne druge tehnologije za izolacijo hmAb iz celic B rekonvalescentov ali cepljenih darovalcev. Veliko protiteles je bilo razvitih in testiranih na kliniki za HIV, izboljšana tehnologija pa je omogočila izolacijo protiteles, ki so bila več kot 1000-krat močnejša od tistih, ki so bila prvotno izolirana proti temu patogenu [148]. V tem okolju je Wellcome Trust leta 2019 objavil poročilo, v katerem navaja, da je čas za razvoj hmAbs za nalezljive bolezni zrel (Wellcome Trust. »Expanding Access to Monoclonal Antibody-Based Products.« (2020)).
Takoj ko se je začela pandemija SARS-CoV-2, je več akademskih in industrijskih laboratorijev izoliralo celice B iz rekonvalescentov in ustvarilo številne publikacije v prestižnih revijah, ki prikazujejo identifikacijo hmAbs, ki lahko nevtralizirajo virus in vitro in ščitijo in zdravljenje miši, hrčkov in primatov razen človeka in vivo pred virusnim izzivom [149]. Nevtralizirajoča protitelesa so običajno razdeljena v štiri razrede, ki vežejo različne predele konice, slika 5. Poleg predkliničnih dokazov je več kliničnih študij pokazalo, da so bila hmAbs zelo učinkovita pri preprečevanju hudih bolezni, če so bila uporabljena zgodaj po okužbi [ 150]. Glede na njihovo učinkovitost in ker so bile to prve terapevtske molekule, razvite med pandemijo, so številna hmAb prejela nujno uporabo v ZDA in Evropi: REGN COV2 (Casirivimab in Imdevimab), Bamlanivimab (LYCoV555), Sotrovimab (VIR 7831 ali S309), Evusheld (tiksagevimab in cilgavimab) in bebtelovimab (LY-CoV1404) [150]. Več kot eno leto so hmAbs ostali edino pravo terapevtsko orodje, ki smo ga imeli proti SARS-CoV-2. Na žalost hmAbs niso delovala v terapevtskem okolju med napredovalo hudo boleznijo pri hospitaliziranih bolnikih in številnim od njih ni uspelo zaradi pojava različic SARSCoV-2, ki prenašajo različne mutacije na koničastem proteinu, glavni tarči za nevtralizacijo hmAbs. Pravzaprav je s pojavom različice SARS-CoV-2 Omicron 85 % domov, odobrenih za klinično uporabo, izgubilo moč proti temu virusu [151]. Danes imamo še vedno tri odobrena hmAb, ki razmeroma dobro delujejo proti omikronu, v literaturi pa so opisana nova močna monoklonska zdravila proti tej različici [151]. Skratka, pandemija COVID-19 je nakazala preventivni in terapevtski potencial hmAbs za nalezljive bolezni, ki jih je mogoče razviti hitreje kot katero koli drugo zdravilo. Poleg tega je zdaj mogoče razviti izjemno močna zelišča, ki jih je mogoče dajati intramuskularno namesto intravensko, kar olajša njihovo dajanje zunaj bolnišnice. Zato se lahko ljudje štejejo za vodilne v medicinskih intervencijah na področju nalezljivih bolezni, saj so zaradi svojih značilnosti bistveno orodje za boj proti nastajajočim patogenom in pandemijam.
CEPLJENJE PROTI SARS-COV-2
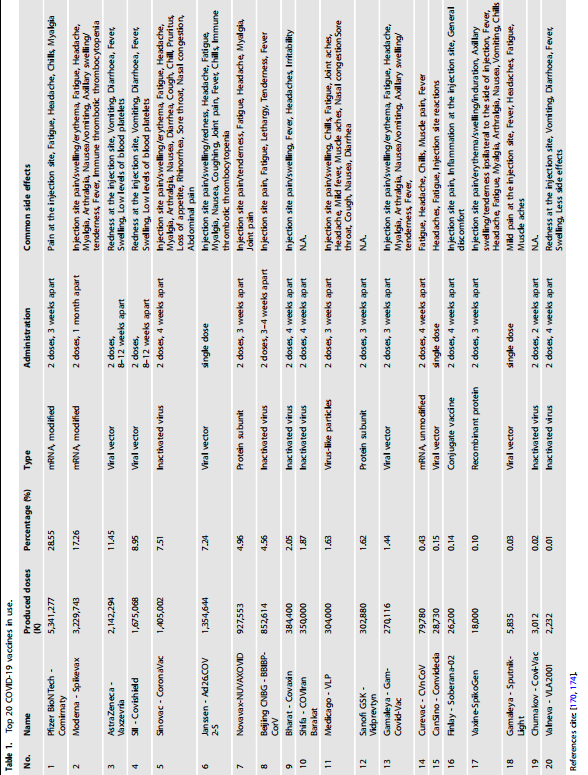
Izpostavljenost oslabljenim patogenom ali delom patogenov za induciranje specifične imunosti proti patogenu se je začela z variacijo črnih koz na Kitajskem pred več kot 1,{1}} leti [152]. Edward Jenner je 800 let pozneje uporabil kravje koze za zaščito ljudi pred črnimi kozami. Ker je v latinščini beseda Vacca za kravo, je izraz cepljenje pozneje prilagodil Jennerjev prijatelj Richard Dunning leta 1800. V zadnjih 200 letih so se razvili različni pristopi za zaščito ljudi pred različnimi okužbami s cepljenjem. Eden najbolj impresivnih rezultatov sodobne medicine je razvoj zelo učinkovitih cepiv proti SARS-CoV-2 v manj kot enem letu od začetka pandemije, slika 6. Od pojava SARSCoV{{9} } so znanstveniki preizkušali različne načine za razvoj cepiv in najpomembnejši vključujejo modificirano mRNA, ki kodira S-protein (Moderna in BioNTech), replikacijsko okvarjen virusni vektor, ki vsebuje zaporedje S-proteina (Ad5-nCov-CanSino , AZD1222-A-AstraZeneca, GRAD-COV2-Reithera na osnovi ChAdOx1), inaktivirani patogeni SARS-CoV-2 (SinoVac, SinoPharm) in rekombinantne beljakovine virusne podenote (celoten S-protein ali RBD), tabela 1. Med 10 milijardami dostavljenih odmerkov zasedajo do sedaj več kot 95 % trga cepiva mRNA podjetij BioNTech in Moderna ter cepivo na osnovi virusnih vektorjev podjetja AstraZeneca in inaktivirana cepiva podjetij Sinovac in Sinopharm.
Zaradi izrednih razmer zaradi pandemije COVID{0}} so imeli znanstveniki minimalno dovolj časa, da ocenijo učinkovitost razvitih cepiv, in obstaja veliko možnosti za izboljšave. Na primer, interval med odmerki (21 dni za Pfifizer; 28 dni za Moderno) se zdi prekratek, razumevanje kratkotrajnega odziva protiteles (6 mesecev) pa je še vedno nedosegljivo. Navzkrižna reaktivnost s SARS in MERS lahko nakazuje možnost univerzalnega pan-koronavirusnega cepiva. Poleg tega, tako kot pri drugih cepljenjih, obstaja možnost, da posebna komenzalna mikrobiota, helminti, hranila (žolčne kisline, butirati) ali antibiotiki, da ne omenjamo imunosupresivnega statusa, oslabijo imunski odziv. Doslej sta za oceno učinkovitosti cepiva najbolj priljubljeni dve metodi, raven protiteles in zaščita pred okužbo v realnem svetu. Jasno je, da je protitelo dober napovednik in obstajajo epidemiološki podatki, ki podpirajo dobro korelacijo med ravnijo protiteles in dovzetnostjo za bolezen [153], zlasti glede na kompleksnost razredov protiteles in njihovo kinetiko. Ker lahko cepiva le zmanjšajo resnost, ni dobrega modela in posebnosti za kvantitativno analizo in natančno določitev zaščitnosti.
We have previously hypothesized that "there are many types or subtypes of coronavirus" -or variants. Thus, if vaccines directly targeting SARS-CoV-2 prove to be difficult to develop, the Edward Jenner approach should be considered [154]. It has been noted that a subset of T cells primed against seasonal coronaviruses cross-react with SARS-CoV-2, and this is believed that it may contribute to clinical protection, particularly in early life. The coronaviruses belong to a family of enveloped single-stranded positive-sense RNA viruses. Available information on cellular immunity to other human coronaviruses (HCoVs), especially those causing the common cold, could be valuable for elucidating immunity to SARS-CoV-2. It is estimated that >90 % odraslih je že bilo izpostavljenih virusom prehlada. Ali je celična imunost na druge koronaviruse, kot je SARS-CoV-1, obstojna, je še vedno vprašanje, čeprav je bilo dokazano, da se lahko T-celični odzivi izzovejo po 17 letih [155]. Trajne T-celične odzive so opazili pri nekaterih bolnikih, okuženih z MERS, čeprav jih je treba še preveriti z longitudinalnimi študijami pri več bolnikih. Glede na široko razširjenost podkovnjakov v jugovzhodni Aziji in nizko stopnjo okužbe s SARS-CoV-2 na tem območju (3,1 % v jugovzhodni Aziji, 14,9 % v Ameriki in 22,5 % v Evropi po podatkih WHO Nadzorna plošča COVID-19 od februarja 2022), je domnevno, da lahko nekateri koronavirusi netopirjev zagotovijo naravno imunost domačim prebivalcem. Kot je storil Edward Jenner z virusom kravjih koz, da bi zaščitil ljudi pred črnimi kozami, lahko poskusimo identificirati koronavirus netopirjev, da bi zaščitili ljudi pred SARS-CoV-2. Uspešno cepivo je odvisno od različnih dejavnikov, kot so identifikacija učinkovitih epitopov ali virusnih komponent, dostavnih vektorjev, ustreznega adjuvansa, poti dajanja ter fizičnega in zdravstvenega stanja prejemnikov [156]. Tudi če imamo učinkovita cepiva, lahko stopnja cepljenja v določenem času, družbena sprejemljivost/odpornost in neustrezna socialna distanca omogočijo virusu dovolj dolgo prisotnost v populaciji, da mutira [157]. Trenutno se zdi, da nobena od razpoložljivih formulacij cepiva ne more popolnoma preprečiti okužbe z virusom, vsaj ko gre za zelo nalezljive različice, kot je različica Omicron. Kar je treba upoštevati v teh okoliščinah s pogosto le delnimi imunskimi zaščitnimi pogoji, je, da je virus izpostavljen neugodnim razmeram, ki lahko povzročijo mutacijo virusa.

Slika 6 Heterologne strategije začetnega pospeševanja z inaktiviranim cepivom (1.) in cepivom mRNA (2.) zagotavljajo močno zaščito pred SARS-CoV-2. Inaktivirano cepivo SARS-CoV-2 rezervira vse virusne beljakovine za imunsko prepoznavanje. Ko so imunizirani, lahko ti antigeni izzovejo skupino T-pomočnikov, ki široko cilja na proteine SARS-CoV-2. Po drugi strani pa mRNA cepivo izzove močan humoralni in celični imunski odziv proti različicam SARS-CoV-2 pri posameznikih, ki so predhodno prejeli inaktivirano cepivo. Domnevali smo, da bi se skupina T-pomočnikov, pripravljena z inaktiviranim cepivom, lahko aktivirala po cepljenju z mRNA, kar olajša izgradnjo močnejšega imunskega odziva in spomina.
KAJ BO SLEDILO OMICRONU
Med vsemi različicami SARS-CoV-2 Omicron prinaša največ skrbi, zmede in pričakovanj. Hitra stopnja prenosa različice Omicron je sprožila resne pomisleke med epidemiologi, politiki in strokovnjaki za nadzor bolezni, odkar so 24. novembra 2021 prvič poročali iz Južne Afrike [158]. K hitremu širjenju prispeva veliko dejavnikov. Možno je, da se virus začne širiti kmalu po začetni okužbi in veliko pred pojavom simptomov. Omicron je približno 10-krat bolj nalezljiv kot divji tip SARS-CoV-2 ali 2,8-krat bolj nalezljiv kot Delta. Novonastali Omicron BA.2 je še bolj nalezljiv [159]. Analiza mutacij Omikrona in njegovih različic BA.2 kaže, da njihovi koničasti proteini nosijo velike količine mutacij, veliko več kot prejšnji VoC, slika 1. Od mutacij je D614G dobro znana mutacija, ki zagotavlja povečano infektivnost z več mehanizmi, vključno z bimodularni vpliv na stabilnost trimerja konic [160, 161]; verjeli so, da mutacije v K417 in E484 regije RBD spreminjajo afiniteto konic do ACE2 [162]; dokazano je, da mutacija N501Y spreminja tropizem virusa tako, da omogoči prenos med vrstami na miši [163], s čimer ustvari potencialnega vmesnega gostitelja, ki pomaga pri širjenju virusa [164]. Najnovejše študije so dejansko odkrile okužbo z omikronom pri podganah in miših [165–167], kar podpira zoonotski prenos nove zaskrbljujoče različice SARS-CoV-2. Pričakuje se, da so mutacije v Omicron RBD skupaj spremenile afiniteto do ACE2, vendar analiza strukture beljakovin ni odkrila višje afinitete [168]. Dejavniki, ki prispevajo k zelo nalezljivi naravi, ostajajo skrivnost. Kljub temu sta visoka sposobnost širjenja in navidezno manjša patogenost vzbudila upanje na kolektivno imunost in konec pandemije. Vprašanje je, ali je omikron zdaj res manj patogen, vendar lahko pridobi povečano patogenost z nadaljnjimi mutacijami.
Nobenega zagotovila ni, da bo naslednja varianta milejša. Najbolj zaskrbljujoč je pojav Deltacrona, ki ima hrbtenico različice Delta in konico Omicron. Informacije o hitrosti prenosa in patogenosti Deltacrona so nujno potrebne. Veliko je razprav o učinkovitosti obstoječih cepiv proti omikronu. Skoraj vso imunost, ki jo povzroča cepivo, bi lahko napadla različica Omicron. Zaradi manjše sposobnosti indukcije protiteles naj bi inaktivirana cepiva ne bila tako učinkovita pri zagotavljanju zaščite pred okužbo. Znanstveniki čakajo na najnovejše podatke o resnosti bolezni bolnikov, okuženih z omikronom, iz celinske Kitajske, kjer jih je skoraj 90 % prejelo inaktivirana cepiva, in iz Hong Konga, kjer je večina ljudi cepljena s cepivi RNK. Treba je opozoriti, da je večnacionalna študija pokazala, da so prejemniki, ki so bili najprej cepljeni z inaktiviranim cepivom, ki mu je sledilo cepivo RNA, pokazali največ protiteles, specifičnih za RBD, in celic T, specifičnih za Omicron, v primerjavi z dvema imunizacijama z eno vrsto cepiva. Inaktivirano cepivo inducira več celic T pomočnic, ker ga predstavlja MHC razreda II, slika 6. Poročalo se je, da heterologna imunizacija z inaktiviranim cepivom, ki ji sledi spodbujevalnik mRNA, izzove močan humoralni in celični imunski odziv proti SARS-CoV{ {6}} Različica omikron [169]. Končno, kako se bo končala pandemija COVID-19? Bo omikron zadnja različica? Če ne, kakšne lastnosti bo imela naslednja varianta? Največje vprašanje je, ali bo COVID-19 postal endemičen. Upamo samo, da z imunostjo, zgrajeno s cepljenjem in okužbo prebivalstva, endemija ni tako smrtonosna. Jasno je, da se moramo naučiti novih rutin SARS-CoV-2.
REFERENCE
1. Chen J, Lu H, Melino G, Boccia S, Piacentini M, Ricciardi W, et al. Okužba s COVID-19: perspektiva Kitajske in Italije. Cell Death Dis. 2020; 11: 438.
2. Ackermann M, Anders HJ, Bilyy R, Bowlin GL, Daniel C, De Lorenzo R, et al. Bolniki s COVID-19: v temi-NET nevtrofilcev. Celična smrt se razlikuje. 2021; 28: 3125–39.
3. Goubet AG, Dubuisson A, Geraud A, Danlos FX, Terrisse S, Silva CAC, et al. Podaljšano izločanje RNA virusa SARS-CoV-2 in limfopenija sta znaka COVID-19 pri bolnikih z rakom s slabo prognozo. Celična smrt se razlikuje. 2021; 28: 3297–315.
4. Matsuyama T, Kubli SP, Yoshinaga SK, Pfeffer K, Mak TW. Nenormalna pot STAT je osrednjega pomena za COVID-19. Celična smrt se razlikuje. 2020; 27: 3209–25.
5. Matsuyama T, Yoshinaga SK, Shibue K, Mak TW. Pomanjkanje glutamina, povezano s komorbidnostjo, je nagnjenost k hudi bolezni COVID-19. Celična smrt se razlikuje. 2021; 28: 3199–213.
6. Verkhratsky A, Li Q, Melino S, Melino G, Shi Y. Ali lahko pandemija COVID-19 poveča epidemijo nevrodegenerativnih bolezni? Biol Direct. 2020; 15:28.
7. Murray CJL, Piot P. Potencialna prihodnost pandemije COVID{1}}: Ali bo SARSCoV-2 postal ponavljajoča se sezonska okužba? JAMA. 2021; 325: 1249–50.
8. Buonvino S, Melino S. New Consensus pattern in Spike CoV-2: možne posledice v procesu koagulacije in fuziji med celicami. Cell Death Disco. 2020; 6: 134.
9. Colson P, Fournier PE, Delerce J, Million M, Bedotto M, Houhamdi L, et al. Kultura in identifikacija »Deltamicron« SARS-CoV-2 v skupini treh primerov v južni Franciji. J Med Virol. 2022. Na spletu pred tiskom.
10. Forni G, Mantovani A. Covid-19 Komisija Accademia Nazionale dei Lincei R. COVID-19 cepiva: kje smo in izzivi pred nami. Celična smrt se razlikuje. 2021; 28: 626–39.
11. Lin L, Wang Y, Li Q, Hu M, Shi Y. Nove terapevtske tarče SARS-CoV-2: lektorski kompleks RNK in staranje, povzročeno z virusom. Celična smrt se razlikuje. 2022; 29: 263–5.
12. Shi Y, Wang Y, Shao C, Huang J, Gan J, Huang X, et al. Okužba s COVID-19: pogledi na imunske odzive. Celična smrt se razlikuje. 2020; 27: 1451–4.
13. Mauriello A, Scimeca M, Amelio I, Massoud R, Novelli A, Di Lorenzo F, et al. Trombembolija po cepivu proti COVID-19 pri bolnikih z obstoječo trombocitopenijo. Cell Death Dis. 2021; 12: 762.
14. Telenti A, Arvin A, Corey L, Corti D, Diamond MS, Garcia-Sastre A, et al. Po pandemiji: pogledi na prihodnjo pot COVID-19. Narava. 2021; 596: 495–504.
15. Sacco G, Briere O, Asfar M, Guerin O, Berrut G, Annweiler C. Simptomi COVID-19 med starejšimi odraslimi: sistematičen pregled biomedicinske literature. Geriatr. Psychol Neuropsychiatr Vieil. 2020; 18: 135–9.
16. Dehingia N, Raj A. Spolne razlike v smrtnosti primerov COVID-19: ali vemo dovolj? Lanceta. Glob Zdravje. 2021; 9: e14–e5.
17. Flaherty GT, Hession P, Liew CH, Lim BCW, Leong TK, Lim V, et al. COVID-19 pri odraslih bolnikih z že obstoječo kronično boleznijo srca, dihal in presnovo: kritičen pregled literature s kliničnimi priporočili. Cepiva Trop Dis Travel Med. 2020; 6:16.
18. Karim SSA, Karim QA. Različica Omicron SARS-CoV-2: novo poglavje v pandemiji COVID-19. Lanceta. 2021; 398: 2126–8.
19. Kozlov M. Šibak napad Omikrona na pljuča bi ga lahko naredil manj nevarnega. Narava. 2022;601:177.
20. Wolter N, Jassat W, Walaza S, Welch R, Moultrie H, Groome M, et al. Zgodnja ocena klinične resnosti različice omikron SARS-CoV-2 v Južni Afriki: študija povezovanja podatkov. Lanceta. 2022; 399: 437–46.
21. Irving AT, Ahn M, Goh G, Anderson DE, Wang LF. Lekcije iz gostiteljske obrambe netopirjev, edinstvenega virusnega rezervoarja. Narava. 2021; 589: 363–70.
22. Burki TK. Različica omikrona in obnovitvena cepiva proti COVID-19. Lancet Respir Med. 2022;10:e17.
23. Junqueira C, Crespo A, Ranjbar S, de Lacerda LB, Lewandrowski M, Ingber J, et al. Okužba monocitov s SARS-CoV-2, posredovana s FcgammaR, aktivira vnetje. Narava. 2022. Na spletu pred tiskom.
24. Moncunill G, župan A, Santano R, Jimenez A, Vidal M, Tortajada M, et al. Seroprevalenca SARSCoV-2 in kinetika protiteles med zdravstvenimi delavci v španski bolnišnici po 3 mesecih spremljanja. J Infect Dis. 2021; 223: 62–71.
25. Zipeto D, Palmeira JDF, Arganaraz GA, Arganaraz ER. Medsebojno delovanje ACE2/ADAM17/TMPRSS2 je lahko glavni dejavnik tveganja za COVID-19. Front Immunol. 2020; 11: 576745.
26. Callaway E. Znanstveniki so ljudem namenoma dali COVID - tukaj so izvedeli. Narava. 2022; 602: 191–2.
27. Schulte-Schrepping J, Reusch N, Paclik D, Bassler K, Schlickeiser S, Zhang B, et al. Hudo obliko bolezni COVID-19 zaznamuje nereguliran del mieloidnih celic. Celica. 2020; 182: 1419–40 e23.
28. Zhang Q, Bastard P, Liu Z, Le Pen J, Moncada-Velez M, Chen J, et al. Prirojene napake imunosti tipa I IFN pri bolnikih z življenjsko nevarno boleznijo COVID-19. Znanost. 2020;370:eabd4570.
29. Ellinghaus D, Degenhardt F, Bujanda L, Buti M, Albillos A, Invernizzi P, et al. Raziskava genomske povezave hude oblike bolezni COVID-19 z odpovedjo dihanja. N Engl J Med. 2020; 383: 1522–34.
30. Delorey TM, Ziegler CGK, Heimberg G, Normand R, Yang Y, Segerstolpe A, et al. Atlasi tkiv COVID-19 razkrivajo patologijo SARS-CoV-2 in celične tarče. Narava. 2021; 595: 107–13.
31. Schultze JL, Aschenbrenner AC. COVID-19 in človeški prirojeni imunski sistem. Celica. 2021; 184: 1671–92.
32. Salvi V, Nguyen HO, Sozio F, Schioppa T, Gaudenzi C, Laffranchi M, et al. SARSCoV-2-povezane ssRNA aktivirajo vnetje in imunost prek TLR7/8. JCI Insight. 2021; 6: e150542.
33. van der Made CI, Simons A, Schuurs-Hoeijmakers J, van den Heuvel G, Mantere T, Kersten S, et al. Prisotnost genetskih različic pri mladih moških s hudo obliko bolezni COVID-19. JAMA. 2020; 324: 663–73.
34. Lu Q, Liu J, Zhao S, Gomez Castro MF, Laurent-Rolle M, Dong J, et al. SARS-CoV-2 poslabša vnetne odzive v mieloidnih celicah prek lektinskih receptorjev tipa C in člana družine Tweety 2. Imunost. 2021; 54: 1304–19 e9.
35. Lempp FA, Soriaga LB, Montiel-Ruiz M, Benigni F, Noack J, Park YJ, et al. Lektini okrepijo okužbo s SARS-CoV-2 in vplivajo na nevtralizirajoča protitelesa. Narava. 2021; 598: 342–7.
36. Stravalaci M, Pagani I, Paraboschi EM, Pedotti M, Doni A, Scavello F, et al. Prepoznavanje in zaviranje SARS-CoV-2 s humoralnimi molekulami za prepoznavanje vzorcev prirojene imunosti. Nat Immunol. 2022; 23: 275–86.
37. Chiodo F, Bruijns S, Rodriguez E, Eveline Li RJ, Molinaro A, Silipo A, et al. Nova ACE2-neodvisna vezava ogljikovih hidratov koničastega proteina SARS-CoV-2 za gostovanje lektinov in pljučne mikrobiote. Prednatis na https://www.biorxiv.org/content/ 10.1101/2020.05.13.092478v1. 2020.
38. Muus C, Luecken MD, Eraslan G, Sikkema L, Waghray A, Heimberg G, et al. Enocelična metaanaliza vstopnih genov SARS-CoV-2 v tkiva in demografske podatke. Nat Med. 2021; 27: 546–59.
39. Grant RA, Morales-Nebreda L, Markov NS, Swaminathan S, Querrey M, Guzman ER, et al. Vezi med okuženimi makrofagi in celicami T pri pljučnici SARS-CoV-2. Narava. 2021; 590: 635–41.
40. van Beek AA, Van den Bossche J, Mastroberardino PG, de Winther MPJ, Leenen PJM. Presnovne spremembe v starajočih se makrofagih: sestavine vnetja? Trendi Immunol. 2019; 40: 113–27.
41. Locati M, Curtale G, Mantovani A. Raznolikost, mehanizmi in pomen plastičnosti makrofagov. Annu Rev Pathol. 2020; 15: 123–47.
42. Xue J, Schmidt SV, Sander J, Draffehn A, Krebs W, Quester I, et al. Mrežna analiza na podlagi transkriptoma razkriva model spektra aktivacije človeških makrofagov. Imuniteta. 2014; 40: 274–88.
43. Mantovani A, Netea MG. Izurjena prirojena imunost, epigenetika in Covid-19. N Engl J Med. 2020; 383: 1078–80.
44. Habibzadeh F, Sajadi MM, Chumakov K, Yadollahie M, Kottilil S, Simi A, et al. Okužba s COVID-19 med ženskami v Iranu, ki so bile izpostavljene, v primerjavi z neizpostavljenimi otroki, ki so prejeli oslabljeni poliovirus, uporabljen v peroralnem cepivu proti otroški paralizi. JAMA Netw Open. 2021;4:e2135044.
45. Wendisch D, Dietrich O, Mari T, von Stillfried S, Ibarra IL, Mittermaier M, et al. Okužba s SARS-CoV-2 sproži profibrotične odzive makrofagov in pljučno fibrozo. Celica. 2021; 184: 6243–61 e27.
46. Kramer B, Knoll R, Bonaguro L, ToVinh M, Raabe J, Astaburuaga-Garcia R, et al. Zgodnji podpisi IFN-alfa in vztrajna disfunkcija so značilne lastnosti celic NK pri hudi bolezni COVID-19. Imuniteta. 2021; 54: 2650–69 e14.
47. Witkowski M, Tizian C, Ferreira-Gomes M, Niemeyer D, Jones TC, Heinrich F, et al. Nepravočasni odzivi TGFbeta pri COVID-19 omejujejo protivirusne funkcije celic NK. Narava. 2021; 600: 295–301.
48. Bernardes JP, Mishra N, Tran F, Bahmer T, Best L, Blase JI, et al. Longitudinalne multiomične analize prepoznajo odzive megakariocitov, eritroidnih celic in plazmablastov kot znake hudega COVID-a-19. Imuniteta. 2020; 53: 1296–314 e9.
49. Georg P, Astaburuaga-Garcia R, Bonaguro L, Brumhard S, Michalick L, Lippert LJ, et al. Aktivacija komplementa povzroči čezmerno citotoksičnost celic T pri hudi bolezni COVID-19. Celica. 2022; 185: 493–512 e25.
50. Bottazzi B, Doni A, Garlanda C, Mantovani A. Integriran pogled na humoralno prirojeno imunost: pentraksini kot paradigma. Annu Rev Immunol. 2010; 28: 157–83.
51. Garlanda C, Bottazzi B, Magrini E, Inforzato A, Mantovani A. PTX3, humoralna molekula za prepoznavanje vzorcev, pri prirojeni imunosti, popravljanju tkiv in raku. Physiol Rev. 2018; 98: 623–39.
52. Brunetta E, Folci M, Bottazzi B, De Santis M, Gritti G, Protti A, et al. Izražanje makrofagov in prognostični pomen dolgega pentraksina PTX3 pri COVID-19. Nat Immunol. 2021; 22: 19–24.
53. Gritti G, Raimondi F, Bottazzi B, Ripamonti D, Riva I, Landi F, et al. Siltuksimab znižuje uravnavanje interlevkina-8 in pentraksina-3 za izboljšanje stanja ventilacije in preživetja pri hudi bolezni COVID-19. levkemija. 2021; 35: 2710–4.
54. Gutmann C, Takov K, Burnap SA, Singh B, Ali H, Theofifilatos K, et al. RNKemija SARS-CoV-2 in proteomske trajektorije dajejo informacije o napovedi pri bolnikih s COVID-19, sprejetimi na intenzivno nego. Nat Commun. 2021;12:3406.
55. Hansen FC, Nadeem A, Browning KL, Campana M, Schmidtchen A, van der Plas MJA. Diferencialna internalizacija gostiteljskih obrambnih peptidov, pridobljenih iz trombina, v monocite in makrofage. J Prirojena imunost. 2021: 1–15.
56. Schirinzi A, Pesce F, Laterza R, D'Alise MG, Lovero R, Fontana A, et al. Pentraksin 3: potencialna prognostična vloga pri bolnikih s SARS-CoV-2, sprejetimi na urgentni oddelek. J Okuži. 2021; 82: 84–123.






