5. del: Preslikava epigenomskega in transkriptomskega medsebojnega delovanja med tvorbo spomina in priklicem v ansamblu hipokampalnega engrama
Mar 22, 2022
ali.ma@wecistanche.com

Razširjeni podatki Slika 2: Stabilni DAR-ji so pretežno obogateni z oznakami ojačevalcev
(a) Potek dela za disekcijo s pretočno citometrijo različnih nevronskih populacij iz hipokampusa medspominoblikovanje in pridobivanje. Reprezentativne ploskve FACS, ki prikazujejo izražanje celotne populacije (leva plošča). Nadaljnji izbor je bil narejen na posameznih jedrih in populaciji NeuN plus /DAPI plus (srednja plošča). Nazadnje je bil izbor opravljen na zaprti podpopulaciji; GFP plus (prilagojen na ~2,5 odstotka od vseh celic), ARC plus /GFP plus (~0.15 odstotkov od vseh celic) in jedra so bila razvrščena v 1,5 ml Eppendorfove epruvete, prevlečene z 200 ul 1-odstotnega PBS.

Kliknite zaIzvleček cistanke v prahu izboljša spomin
(b) Vennov diagram (levo) in tabela (desno) ponazarjata prekrivanje med DAR-ji, ugotovljenimi v različnih parnih primerjavah medspominoblikovanje in odpoklic.
(c) Opravljena je bila statistična analiza na podlagi ponovnega vzorčenja, da se ugotovi, ali so obogatitve stanj kromatina nad emisijami ChromHMM (opažene) statistično pomembne. Pričakovana obogatitev je bila izračunana z izvedbo 10,000 randomiziranih nizov prekrivanj (permutacij) med 'vsemi dostopnimi mesti' in 'vsemi mesti modifikacije histonov (tj. vse emisije)' lokusi in predstavljena kot histogram v postava. Velikost vzorca vsakega randomiziranega niza je bila določena z velikostjo DAR iz vsake države. Izračunana sta bila povprečje in standardni odklon vzorca (dodatna tabela 3). Število opaženih prekrivanj med DAR in vsako emisijo je bilo izračunano in predstavljeno kot črte. z-rezultat je bil izračunan kot prah; Z=(opazovane vrednosti (X) – povprečje vzorca (μ))/(standardni odklon vzorca (σ)). z-rezultat bazalni v primerjavi z zgodnjim; JV 10.5, SR 6.9. Stabilen; SE 16,9, WE 12,7, vsi p < 0,0001,="" z-rezultat="" early="" vs.="" late;="" sp="" 91.7,="" wp="" 38.7.="" pozno="" proti="" ponovno="" aktiviranemu;="" sp="" 26.8,="" wp="" 28.9,="" vse=""><0.0001. p-values="" (two-sided)="" were="" calculated="" from="" the="" z-table.="" a="" full="" analysis="" is="" reported="" in="" supplement="" table="">

(d) Tortni grafikon prikazuje odstotek različnih stanj ojačevalca za vse stabilne regije. Prekrivanje vsake stabilne regije je bilo izvedeno s predhodno objavljenimi podatki H3K4me1 in H3K27ac ChIP-seq, pridobljenimi 1 uro po FS21. Stanja ojačevalcev so bila razvrščena kot „pripravljena“ – prekrivajo se z regijami, označenimi samo s H3K4me1, „aktivna“ – s H3K4me1/H3K27ac ali „latentna“ – brez prekrivanja.
(e) Motifs identified from nucleosome-free regions (NFR) on the ATAC-seq tracks from each state (Basal, Activated -early, Activated -late, and Reactivated). Peaks were divided into positions that were annotated to promoters (5kb from TSS) and enhancers (>5kb iz TSS). Velikost kroga označuje odstotek obogatitve (1–50 odstotkov). Barva označuje –log(P-vrednost).

Razširjeni podatki Slika 3: Usklajeno pripravo epigenetskega stanja medspominkodiranje in
(a) Lastnosti Chicago zaznanih interakcij v vsaki fazi (bazalna, aktivirana - zgodaj, aktivirana - pozno in ponovno aktivirana). Privzete nastavitve in rezultatski prag 5 so bili uporabljeni pri klicu pomembne interakcije, izvedenem skupaj na vseh ponovitvah.
(b) Tortni grafikon predstavlja odstotek vseh interakcij, odkritih v Chicagu, ki so razmejene s H3K27ac/H3K4me1 (67,5-odstotne oznake ojačevalcev), H3K4me3/H3K9ac (46,2-odstotna oznaka promotorjev) ali H3K27me3 (1,1-odstotne oznake za represijo).
(c) Slika brskalnika epigenoma WashU, ki zajema ~ 500 Kb regijo okoli genov Eif4e2. Loki prikazujejo pomembne skupne (rdeči pravokotnik) in edinstvene (puščice) ojačevalce, ki medsebojno delujejo s promotorji (modri pravokotnik).

(d) Primeri interakcij, ki jih imenuje Chicago. Grafi, ki prikazujejo vsa števila branja iz bait-other-end (enhancer), znotraj 500–700 kb (gorvodno in dolvodno) od Grink3 in Promotorji Wwc2. Pomembne interakcije, ki jih je zaznal Chicago (rezultat večji ali enak 5), so prikazane rdeče, interakcije pod pragom (3 manj kot ali enak rezultatu < 5)="" pa="" modro.="" sive="" črte="" prikazujejo="" pričakovano="" število,="" črtkane="" črte="" pa="" zgornjo="" mejo="" 95-odstotnega="" intervala="" zaupanja.="" (e)="" analiza="" obogatitve="" prekrivanja="" med="" medsebojno="" delujočimi="" ojačevalci="" in="" dar-ji="" z="" uporabo="" permutacijskega="" postopka="" na="" 10,000="" randomiziranih="" nizih="" dostopnih="" mest.="" histogram="" predstavlja="" naključno="" vzorčno="" porazdelitev="" dostopnih="" mest="" za="" vsako="" stanje="" (bazalno="" proti="" aktiviranemu="" -="" zgodaj,="" aktivirano="" -="" zgodaj="" proti="" aktiviranemu="" -="" pozno,="" aktivirano="" -="" pozno="" proti="" ponovno="" aktiviranemu,="" stabilno).="" število="" prekrivajočih="" se="" lokusov="" je="" predstavljeno="" v="" barvnih="" črtah="" iz="" bazalnih,="" aktiviranih="" -="" zgodnjih,="" aktiviranih="" -="" poznih="" in="" reaktiviranih="" nevronov.="" dar="" za="" bas="" v="" primerjavi="" z="" aktiviranim="" -zgodnjim="" (z-ocena;="" 7,1,="" 7,7,="" 8,5,="" 10.9).="" dar="" aktiviranega="" -zgodaj="" v="" primerjavi="" z="" aktiviranim="" -pozno="" (rezultat="" z;="" -0,1,="" -0,8,="" -2,4,="" -3,2).="" dar="" za="" aktivirano="" -pozno="" v="" primerjavi="" z="" reaktivirano="" (0,4,="" 1,8,="" 0,4,="" -0,2).="" dar="" stabilni="" (z-ocena;="" 1,7,="" 2,0,="" 6,5,="">
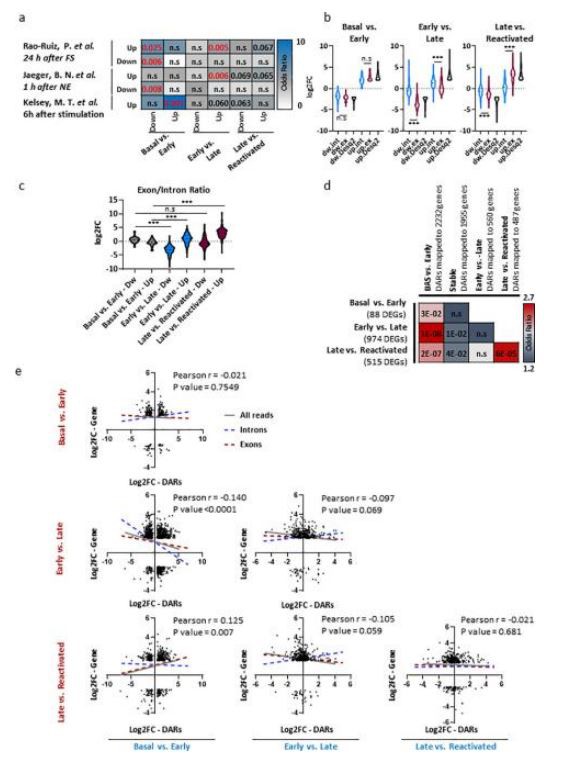
Razširjeni podatki Slika 4: Spremembe kromatina, ki se pojavijo med zgodnjo fazo omogočajo
(a) Analiza prekrivanja med imeni genov iz diferencialne analize po parih in predhodno objavljenih podatkov i) aktiviranih zrnatih celic DG 1 uro po novi izpostavljenosti32 ii) 24 ur po FS20 in iii) po podaljšani stimulaciji (6 ur) kortikalne kulture miši nevronov s KCl33. Analiza je bila izvedena s paketom GeneOverlap R.
(b) Eksonični (rdeči) in intronični (modri) odčitki so bili kvantificirani ločeno v vseh pogojih in primerjani s transkripcijsko aktivnostjo, merjeno z DEseq2. Odčitki so bili normalizirani (RPKM) in spremembe log2FC so predstavljene za vsako stanje. violinska ploskev označuje povprečje,
interkvartilni razpon ter najmanjši in največji, enosmerna ANOVA (parametrična, neparna), bazalna proti zgodnji; F (5, 248)=389.9. Zgodnji proti poznemu; F (5, 2374)=2183. Pozno proti ponovno aktiviranemu. F (5, 1357) {{10}}.5, vsi P < 0.0001.="" bonferronijeve="" številne="" primerjave.="" ns="nepomembno," ***p=""><>
(c) Razmerja ekson/intron so bila izmerjena v vsaki skupini v vseh pogojih (lestvica Log2FC). violinski prikaz označuje povprečje, interkvartilni razpon ter najmanjšo in največjo, enosmerno ANOVA (parametrično, neparno), F (5, 1143)=260.2, P<0.0001. bonferroni's="" multiple="" comparisons="" test.="" n.s="non-significant," ***p="" <="">
(d) Analiza prekrivanja med DAR in DEG med različnimispominfaze. DAR-ji na intergenskih in intronskih regijah so bili preslikani na njihove ustrezne gene z interakcijskimi zemljevidi pc-HiC. Analiza prekrivanja je bila izvedena s paketom GeneOverlap R. P-vrednost (številke) in razmerje obetov (barva) iz Fisherjevega natančnega testa sta predstavljena na toplotni karti. ns – ni pomembno.
( e ) Pearsonova korelacija med vrednostmi log2FC DAR in log2FC DEG, ki so bile označene za to regijo (medgenske regije so bile preslikane prek nabora podatkov pc-HiC). Spremembe dostopnosti kromatina so primerjali z razčlenjenimi eksoničnimi odčitki (rdeča črta), introničnimi odčitki (modre črte) in skupnimi transkripcijskimi spremembami (tako intronični kot eksonični odčitki), merjeno z Desq2 (siva črta). Vse vrednosti r in p so navedene v dodatni tabeli 9.

Razširjeni podatki, slika 5: Transkripcijske spremembe v aktiviranih poznih nevronih so korelirale višje
(a) Eksonični (rdeči) in intronični (modri) odčitki so bili kvantificirani ločeno v vseh pogojih za vsako od skupin, opredeljenih na sliki 5B. Odčitki so bili normalizirani (RPKM) in spremembe log2FC so predstavljene za vsako gručo.
(b) Razmerja ekson/intron so bila izmerjena v vsaki skupini v vseh pogojih. Violinski graf označuje povprečje, interkvartilni razpon ter minimum in maksimum, n=3 biološko neodvisnih vzorcev, enosmerna ANOVA (parametrična, neparna), Dw – pozni grozd; F (3, 968)
652) = 93.97, P<0.0001. reactivation="" -cluster;="" f="" (3,="" 1600)="485.2,"><0.0001. bonferroni's="" multiple="" comparisons="" test="" to="" deseq2="" reads.="" ***p="" <="">

Razširjeno podatki sl. 6: Izrazit začasno transkripcijska programov so biti sinhronizirano do
odvisen način v prisotnosti tamoksifena. Na desni plošči reprezentativne slike IHC DG. Zelena – AAV-eYFP, rdeča – endogeni lok. Lestvica predstavlja 50 μm.
(b) Ocena morfologije hrbtenice med različnimispominfaze. Desna plošča prikazuje eno samo eYFP plus dendritično steblo z različnimi vrstami bodic (Črtasta, Tanka, Gobasta, Povečana goba). Lestvica predstavlja 5 μm. boxplot označuje povprečje, interkvartilni razpon ter minimum in maksimum, Aktivirano -zgodaj: n=4 miši /5 odsekov na žival, Aktivirano -pozno: n=4 miši /4 odseki na žival, Ponovno aktivirano: n=4 miši /2 odsek na žival. enosmerna ANOVA (parametrična, neparna), Stubby; F (2, 36)=2.313, P=0.1135. tanek; F (2, 36)=35.12, str<0.0001. mushroom;="" f="" (2,="" 36)="38.42," p="" <="" 0.0001.="" bonferroni's="" multiple="" comparisons="" test,="" ***p="" <="">
(c) Reprezentativne slike IHC in kvantifikacija ravni beljakovin dveh članov družine EIF; (levo) Eif2a in (desno) Eif3e. Vrstica merila predstavlja 10 μm. Podatki za dendritično gred so predstavljeni kot razmerje med številom in dolžino (μM). n=4 miši /5 odsekov na žival, škatlasti prikaz označuje povprečje, interkvartilni razpon ter najmanjšo in največjo, enosmerno ANOVA (parametrično, neparno) z Bonferronijevim testom večkratnih primerjav, ns - ni pomembno, Eif2a Shaft; F (2, 20)=4.484, P=0.0246. Soma; F (2, 21)=19.58, P < 0,0001.="" (aktivirano="" -zgodaj="" v="" primerjavi="" z="" aktivirano="" -pozno="" *p="0.0142," aktivirano="" -zgodaj="" v="" primerjavi="" s="" ponovno="" aktivirano="" *p="">< 0,0001,="" aktivirano="" -pozno="" v="" primerjavi="" z="" ponovno="" aktivirano="" *p="0.0303)." gred="" eif3e;="" f="" (2,="" 14)="1.983," p="0.1745." soma;="" f="" (2,="" 23)="8.309," p="0.0019," (aktivirano="" -zgodaj="" vs.="" ponovno="" aktivirano="" *p="0.0057," aktivirano="" -pozno="" vs.="" ponovno="" aktivirano="" *p="" {{="">
(d) Tortni grafikon prikazuje odstotek povečanih gobastih bodic (Dh Večji ali enak 3Dn) in gobastih bodic iz aktiviranih poznih in reaktiviranih nevronov.
(e) Reprezentativne slike (leva plošča) in kvantifikacija (desna plošča) ravni mRNA Gria1 v različnih fazahspomin. Podatki so predstavljeni kot razmerje med več punktami in dolžino dendritične gredi. Lestvica predstavlja 10 μm. N=4 miši /5 odsekov na žival, okvirček označuje povprečje, interkvartilni razpon ter minimum in maksimum, Shaft; enosmerna ANOVA (parametrična, neparna) F (2, 15)=10.41, P=0.0015. Bonferronijev test večkratnih primerjav, **P=0.0011. spodnja plošča - Soma; enosmerna ANOVA F (2, 12)=0.13, P=0.88.

Razširjeni podatki, slika 7: Interakcije z različnimi kombinatoričnimi ojačevalci vodijo do usmerjenega
(a) Vennovi diagrami prikazujejo odstotek prekrivanja med dostopnostjo kromatina (DAR) v vsehspominfaze (BAS v primerjavi z aktiviranim -zgodnjim, svetlo zelenim mrežnim krogom; aktiviranim -zgodnjim v primerjavi z aktiviranim -poznim, temno zelenim mrežnim krogom; aktiviranim -poznim proti reaktiviranemu, oranžnim mrežnim krogom) in skupne transkripcijske spremembe vseh identificiranih skupin (Dw – pozno, pripravljeno – pozno, stabilno, ponovno aktiviranje, moder mrežni krog). Intergenski in intronski DAR-ji so bili preslikani v njihove ustrezne gene z interakcijskimi zemljevidi pc-HiC. Odstotek prekrivanja je bil izračunan iz vseh identificiranih DEG v grozdih (n=1095).
(b) Analiza prekrivanja med DAR (po parih) in DEG iz vsake skupine. Intergenski in intronski DAR-ji so bili preslikani v njihove ustrezne gene z interakcijskimi zemljevidi pc-HiC.
Analiza prekrivanja je bila izvedena s paketom GeneOverlap R. P-vrednosti in Jaccardove vrednosti (barva) iz Fisherjevega natančnega testa so predstavljene na toplotni karti (levo). Odstotek prekrivanja je bil izračunan iz vseh identificiranih DEG v grozdih (desno).
( c ) Reprezentativna slika kromatina in transkripcijskih sprememb lokusa Gabrb3 iz Dw-pozne skupine. Medtem ko so bile interakcije v zgodnjem stanju med promotorjem in ojačevalci s transkripcijskimi aktivatorji (Ap1), so bile interakcije v poznem stanju s transkripcijskimi represorji (Slug). Zgornje sledi brskalnika genoma IGV (vijolična – bazalna, svetlo zelena – aktivirana – zgodaj, temno zelena – aktivirana – pozno in oranžna – ponovno aktivirana) predstavljajo transkripcijske spremembe (ncRNA-seq), srednje sledi pa prikazujejo dinamiko dostopnosti kromatina (ATAC-seq) na promotor (rdeč pravokotnik) in ojačevalci (siv pravokotnik). Pomembne interakcije promotorja in ojačevalca so predstavljene kot loki (sledi brskalnika WashU). Spodnja steza predstavlja motive, ki so bili identificirani z orodji HOMER (Slug, Ap1 in Rest).
(d) Agregacijske ploskve za posamezne motive. Vrednosti obogatitve (motivi na bp/na vrh) šestih izbranih motivov (dva represorja, dva aktivatorja in dva bivalentna) so bile ocenjene okoli središča vrhov (-/ plus 4000 bp) iz vsake skupine.

Razširjeni podatki Slika 8: Predlagani model dostopnosti kromatina, interakcije promotor-ojačevalec in transkripcijske dinamike hipokampalnih spominskih engramskih nevronov
regije, ki skrivajo motive transkripcijskih aktivatorjev. To reprogramiranje promotorja-ojačevalca povzroči povečano ekspresijo genov, ki domnevno omogoča stabilizacijospomin. Spomnimo se – ponovno aktivirani engramski nevroni so uporabili podmnožico primarnih interakcij med promotorjem in ojačevalcem, kar je povezano s transkripcijskimi spremembami, ki so vključene v transport mRNA do sinaptičnih predelkov in prevajanje beljakovin. Transkripcijski faktor – TF, E(1–3) – različni ojačevalci, ki interagirajo z istim promotorjem, Rdeča - transkripcijski represorji, Modra - transkripcijski aktivatorji.

Dodatno gradivo
Za dodatna gradiva si oglejte spletno različico na PubMed Central.
Zahvala
Zahvaljujemo se E. Niederstu, J. Penneyju, S. Barkerju, RT Stottu, M. Victorju, A. Watsonu, N. Dedicu, E. Lockshinu in članom L.HT Laba za koristno razpravo in predloge. Zahvaljujemo se vodjem laboratorija Y. Zhou, E. McNamara za vzdrževanje kolonije miši. Zahvaljujemo se P. Autissierju (Whitehead Institute) za pomoč pri FACS. Financiranje: ta dela so podprli štipendije NIH RF1AG062377, AF1AG054012, RO1NS102730, RF1AG064321, fundacija JPB, fundacija Alana Down Syndrome Research Foundation, fundacija LuMind Down Syndrome Research Foundation, konzorcij Cure Alzheimer's Fund CIRCUITS ter Robert A in Renee E. Družinska fundacija Belfer LH.T. This work was also supported in part by NIH grants R01AG058002, U01NS110453, R01AG062335, UG3NS115064 to MK and LH.T, and R01AG067151, R01MH109978, U01MH119509, R01HG008155, U24HG009446 to MKVD is supported by an AARF-19-618751 grant from Alzheimer's Association . HSM podpirata Burroughs Wellcome Fund in podoktorska štipendija UNCF-Merck. C. A podpira Fundacija JPB. RMR podpira NIH T32 grant 5T32HD09806. Komplet za pripravo knjižnic Hi-C je prejel kot velikodušno darilo DovetailTM (v.1.03, Dovetail Genomics, Chicago, ZDA). Zahvaljujemo se skupini Dovetail za koristno razpravo in predloge.
